题目内容
1963年在格陵兰Ika峡湾发现一种水合碳酸钙矿物ikaite。它形成于冷的海水中,温度达到8oC即分解为方解石和水。1994年的文献指出:该矿物晶体中的Ca2+ 离子被氧原子包围,其中2个氧原子来自同一个碳酸根离子,其余6个氧原子来自6个水分子。它的单斜晶胞的参数为:a =" 887" pm, b =" 823" pm, c =" 1102" pm, β = 110.2°,密度d =" 1.83" g cm-3,Z = 4。
⑴ 通过计算得出这种晶体的化学式。
⑵ 研究了这种晶体在加压下受热膨胀体积增大的情形,并与冰及钙离子配位数也是8的二水合石膏晶体(gypsum)作了对比,结果如下图所示(纵坐标为相对体积):

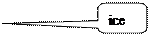

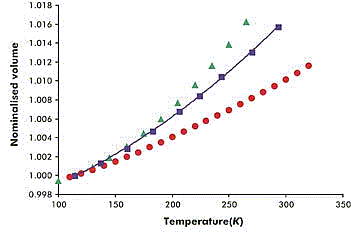
为什么选取冰和二水合石膏作对比?实验结果说明什么?
⑶ 这种晶体属于哪种类型的晶体?简述理由。
⑴ 通过计算得出这种晶体的化学式。
⑵ 研究了这种晶体在加压下受热膨胀体积增大的情形,并与冰及钙离子配位数也是8的二水合石膏晶体(gypsum)作了对比,结果如下图所示(纵坐标为相对体积):



为什么选取冰和二水合石膏作对比?实验结果说明什么?
⑶ 这种晶体属于哪种类型的晶体?简述理由。
⑴ikaite晶胞体积:
V = abc sinβ =" (8.87" ´ 8.23 ´ 11.02 ´ 10-24 cm3) ´ sin110.2° =" 7.55" ´ 10-22 cm3
设晶胞中含有n个水分子,晶胞的质量:m =" 4" ´ (100 + 18 n) / NA (g)
晶体密度:d = m/V =" 4" ´ (100 + 18 n) / ( 6.02 ´ 1023 ´ 7.55 ´ 10-22)(g cm-3)=" 1.83" g cm-3
100 + 18 n =" 208 " n = 6
该晶体的化学式为 CaCO3× 6H2O
⑵Ikaite在冷水中形成,而且含有大量结晶水,分解温度又接近冰的熔点,可能与冰的结构有相似性,故选取冰作参比物;
石膏是带结晶水的钙的含氧酸盐,而且钙的配位数也是8,可能与ikaite结构相似,故选取石膏作参比物。
实验结果说明ikaite的结构跟冰相似。
⑶分子晶体。
晶体分解温度接近冰的熔点,体积随温度的变化趋势也接近冰,可认为晶体中的化学微粒是CaCO3× 6H2O,它们以分子间作用力(氢键和范德华力)构成晶体。
⑴根据题意,设ikaite的化学式为CaCO3·nH2O,利用公式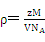 (其中,ρ=abcsinβ),求得摩尔质量M,进而求得n。
(其中,ρ=abcsinβ),求得摩尔质量M,进而求得n。
⑵题中之所以选择这两种物质作类比,是想了解ikaite的结构,因此组成、性质等相似性是类比的基础。从图象上看,由于冰与ikaite体积-温度变化曲线最接近,所以冰与ikaite结构最相似。
⑶从⑵问中可知,该晶体与冰晶体结构最接近,所以晶体类型相同,即同为分子晶体。
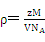 (其中,ρ=abcsinβ),求得摩尔质量M,进而求得n。
(其中,ρ=abcsinβ),求得摩尔质量M,进而求得n。⑵题中之所以选择这两种物质作类比,是想了解ikaite的结构,因此组成、性质等相似性是类比的基础。从图象上看,由于冰与ikaite体积-温度变化曲线最接近,所以冰与ikaite结构最相似。
⑶从⑵问中可知,该晶体与冰晶体结构最接近,所以晶体类型相同,即同为分子晶体。

练习册系列答案
 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案
相关题目