题目内容
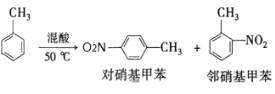
【题目】下图是CO和水蒸气发生反应生成CO2和H2的途径和三个状态的能量,该反应为吸热反应,试问:
E1:CO+H2O![]() E2:C+2H+2O
E2:C+2H+2O![]() E3:CO2+H2
E3:CO2+H2
(1)步骤1、2分别是吸热过程还是放热过程?
步骤1:______,步骤2:______。
(2)比较E1、E3的大小______。
(3)已知,25℃时,C(石墨)+1/2O2(g) ═ CO(g) ΔH1=-111 kJ/mol;
H2(g)+1/2O2(g) ═ H2O(g) ΔH2=-242 kJ/mol;
C(石墨)+O2(g) ═ CO2(g) ΔH3=-394 kJ/mol。
则CO和H2O(g)反应的热化学方程式为:______。
(4)含1 mol Ba(OH)2的稀溶液与足量稀盐酸反应放出114.6 kJ的热量,写出该反应中和热的热化学方程式:______。
(5)在C2H2(g)完全燃烧生成CO2和液态水的反应中,每转移5NA个电子放出a kJ的热量。则表示C2H2的燃烧热的热化学方程式为:______。
【答案】吸热过程 放热过程 E1<E3 CO(g)+H2O(g) ═ CO2(g)+H2(g) ΔH=-41 kJ/mol 1/2Ba(OH)2(aq)+HCl(aq) ═ 1/2BaCl2(aq)+H2O(l) ΔH=-57.3 kJ/mol C2H2(g)+5/2O2(g) ═ 2CO2(g)+H2O(l) ΔH=-2a kJ/mol
【解析】
在化学反应中,断键需要吸热,成键需要放热。在一个吸热反应中,反应物所具有的总能量低于产物所具有的总能量。因此在由CO+H2O生成CO2+H2的反应中E1<E3。在利用盖斯定律进行方程式重组时需注意找寻分式与目标方程式之间的关系,然后列出叠加原则。根据叠加原则将物质变化进行叠加,检查叠加后式子是否与目标式相同,再计算反应热。据此解题。
(1) 步骤1为化学键的断裂过程,需要吸收热量,因此步骤1为吸热过程,步骤2为化学键的形成过程,需要释放能量,因此步骤2为放热过程;
(2)由于CO+H2O生成CO2+H2的反应为吸热反应,因此反应物所具有的总能量低于产物所具有的总能量,因此E1<E3;
(3)根据C(石墨)+1/2O2(g) ═ CO(g) ΔH1=-111 kJ/mol;①
H2(g)+1/2O2(g) ═ H2O(g) ΔH2=-242 kJ/mol;②
C(石墨)+O2(g) ═ CO2(g) ΔH3=-394 kJ/mol;③
可知,CO(g)+H2O(g)= CO2(g)+H2(g)的反应热计算式为:ΔH=-①-②+③=111 kJ/mol+242 kJ/mol-394 kJ/mol=-41 kJ/mol,因此该反应的热化学方程式为:CO(g)+H2O(g) ═ CO2(g)+H2(g) ΔH=-41 kJ/mol;
(4) 在稀溶液中,强酸跟强碱发生中和反应生成1 mol液态水时所释放的热量叫做中和热,因此Ba(OH)2的稀溶液与足量稀盐酸反应中和热的热化学方程式应写为:1/2Ba(OH)2(aq)+HCl(aq) ═ 1/2BaCl2(aq)+H2O(l) ΔH=-57.3 kJ/mol;
(5) 在25℃,100kPa时,1 mol纯物质完全燃烧生成稳定的化合物时所放出的热量,叫做该物质的燃烧热。因此当C2H2(g)完全燃烧时,该反应的方程式为2C2H2+5O2 ![]() 4CO2+2H2O,转移20mol电子,因此当反应中每转移5NA个电子放出a kJ的热量时,C2H2的燃烧热的热化学方程式可写为:C2H2(g)+5/2O2(g) ═ 2CO2(g)+H2O(l) ΔH=-2a kJ/mol。
4CO2+2H2O,转移20mol电子,因此当反应中每转移5NA个电子放出a kJ的热量时,C2H2的燃烧热的热化学方程式可写为:C2H2(g)+5/2O2(g) ═ 2CO2(g)+H2O(l) ΔH=-2a kJ/mol。

【题目】已知化学反应①:Fe(s)+CO2(g)![]() FeO(s)+CO(g),其化学平衡常数为K1;化学反应②:Fe(s)+H2O(g)
FeO(s)+CO(g),其化学平衡常数为K1;化学反应②:Fe(s)+H2O(g)![]() FeO(s)+H2(g),其化学平衡常数为K2,在温度973 K和1173 K的情况下,K1、K2的值分别如下:
FeO(s)+H2(g),其化学平衡常数为K2,在温度973 K和1173 K的情况下,K1、K2的值分别如下:
温度 | K1 | K2 |
973 K | 1.47 | 2.38 |
1 173 K | 2.15 | 1.67 |
(1)通过表格中的数值可以推断:反应①是_______(填“吸热”或“放热”)反应。
(2)现有反应③:CO2(g)+H2(g)![]() CO(g)+H2O(g),请你写出该反应的平衡常数K3的表达式:K3=______。
CO(g)+H2O(g),请你写出该反应的平衡常数K3的表达式:K3=______。
(3)根据反应①与②可推导出K1、K2与K3之间的关系式为__________,据此关系式及上表数据,能推断出反应③是________(填“吸热”或“放热”)反应。
(4)要使反应③在一定条件下建立的平衡向正反应方向移动,可采取的措施有______ 、_____ (填写字母序号)。
A.缩小反应容器的容积 B.扩大反应容器的容积
C.升高温度 D.使用合适的催化剂
E.设法减小平衡体系中的CO的浓度
(5)图甲、乙分别表示反应③在t1时刻达到平衡,在t2时刻因改变某个条件而发生变化的情况:

①图甲中t2时刻发生改变的条件是__________。
②图乙中t2时刻发生改变的条件是__________。