题目内容
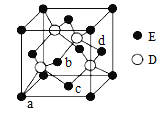
【题目】已知:P4(g)+6Cl2(g)===4PCl3(g) ΔH=a kJ·mol-1,P4(g)+10Cl2(g)===4PCl5(g) ΔH=b kJ·mol-1,又知形成或拆开1 mol化学键放出或吸收的能量称为该化学键的键能。P4具有正四面体形结构,PCl5中P—Cl键的键能为c kJ·mol-1,PCl3中P—Cl键的键能为1.2c kJ·
mol-1。下列叙述正确的是( )
A.P—P键的键能大于P—Cl键的键能
B.可求Cl2(g)+PCl3(g)===PCl5(s)的反应热ΔH
C.Cl—Cl键的键能为![]() kJ·mol-1
kJ·mol-1
D.P—P键的键能为![]() kJ·mol-1
kJ·mol-1
【答案】C
【解析】P—Cl键的键能大于P—P键的键能,A项错误;不知PCl5(g)―→PCl5(s)的能量转化,无法求出B项反应的反应热,B项错误;根据盖斯定律,消去P4,得到Cl—Cl键的键能为![]() kJ·mol-1,C项正确;根据盖斯定律,消去Cl2,得到P—P键的键能为
kJ·mol-1,C项正确;根据盖斯定律,消去Cl2,得到P—P键的键能为![]() kJ·mol-1,D项错误。
kJ·mol-1,D项错误。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目