题目内容
10.相等质量的CO和CH4相比较,请完成下列问题.(1)它们所含的分子数目之比为4:7
(2)同温同压时密度之比为7:4
(3)同温同体积时的压强之比为4:7
(4)同温同压时体积之比为4:7.
分析 根据n=$\frac{m}{M}$可知,相等质量的CO和CH4的物质的量之比为16g/mol:28g/mol=4:7.
(1)分子数目之比等于物质的量之比;
(2)同温同压下,气体的密度之比等于其摩尔质量之比;
(3)同温同体积时,气体的压强之比等于其物质的量之比;
(4)同温同压时,气体体积之比为等于其物质的量之比.
解答 解:根据n=$\frac{m}{M}$可知,相等质量的CO和CH4的物质的量之比为16g/mol:28g/mol=4:7.
(1)分子数目之比等于物质的量之比,相等质量的CO和CH4的所含的分子数目之比为4:7,故答案为:4:7;
(2)同温同压下,气体的密度之比等于其摩尔质量之比,CO和CH4的密度之比为28g/mol:16g/mol=7:4,故答案为:7:4;
(3)同温同体积时,气体的压强之比等于其物质的量之比,二者压强之比为4:7,故答案为:4:7;
(4)同温同压时,气体体积之比为等于其物质的量之比,二者体积之比为4:7,故答案为:4:7.
点评 本题考查阿伏伽德罗定律及其推论,难度不大,注意对基础知识的理解掌握.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
20.下列根据相关实验现象得出的结论正确的是( )
| A. | 某溶液加入盐酸酸化的BaCl2溶液后有白色沉淀生成,该溶液一定含有SO42- | |
| B. | 某气体能能使润湿的淀粉KI试纸变成蓝色,该气体一定是Cl2 | |
| C. | 某溶液中滴加KSCN溶液无明显变化,再滴加氯水后溶液变红色,该溶液中一定含Fe2+ | |
| D. | 将某气体通入溶有足量氨的BaCl2溶液中,有白色沉淀生成,该气体一定是SO2 |
5.下列关于氯气和氯水的说法中正确的是( )
| A. | 氯气是一种无色、密度比空气大的有毒气体 | |
| B. | 红热的铁丝在Cl2中剧烈燃烧生成FeCl2 | |
| C. | 新制氯水能杀菌消毒是因为Cl2有毒,能毒杀细菌 | |
| D. | 氯水放置数天后酸性增强 |
15.下列实验操作中不正确的是( )
| A. | 蒸发操作时,当蒸发到剩有少量液体时,停止加热,利用余热将液体蒸干 | |
| B. | 过滤后洗涤沉淀,是将水沿玻璃棒注入漏斗中,用玻璃棒搅拌后待水流下 | |
| C. | 分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 | |
| D. | 萃取操作时,应选择有机萃取剂,它与原溶剂应不互溶 |
20.一种“人工固氮”的新方法是在常温、常压、光照条件下,N2在催化剂表面与水发生反应生成NH3:N2(g)+3H2O(l)?2NH3(g)+$\frac{3}{2}$O2(g),进一步研究NH3生成量与温度的关系,部分实验数据见下表(反应时间3h):
请回答下列问题:
(1)该反应的平衡常数表达式为$\frac{[N{H}_{3}]^{2}×[{O}_{2}]^{\frac{3}{2}}}{[{N}_{2}]×[{H}_{2}O]^{3}}$.
(2)已知在所给条件下投入1molN2和3molH2O(l),当反应达到平衡时消耗了35kJ的热量,并收集到0.4molNH3.则N2的平衡转化率为20%,该反应的热化学方程式可表示为N2(g)+3H2O(l)?2NH3(g)+$\frac{3}{2}$O2(g)△H=+175.0kJ•mol-1.
(3)与目前广泛应用的工业合成氨方法相比,该方法中固氮反应速率较慢,请提出可提高其反应速率同时增大NH3生成量的措施升高温度、增大氮气浓度.(列出两种即可)
(4)工业合成氨的热化学方程式为N2(g)+3H2(g)?2NH3(g),△H=-92.4kJ•mol-1.在某体积为10L的恒温恒容密闭容器中加入2mol N2和4mol H2,2min后反应达到平衡时容器内的压强是起始压强的2/3.求:
①2min内NH3的反应速率υ(NH3)=0.1 mol/(L•min).
②下列有关该化学反应的说法正确的是B(填字母序号).
A.在恒温恒压条件下,向上述平衡体系中通入少量氩气,平衡不移动
B.在恒温恒容条件下,向上述平衡体系中通入少量氩气,平衡不移动
C.实际工业生产中为提高H2的转化率,通常通入过量的N2,且N2过量越多越好
D.当温度、体积相同且恒定不变时,向甲容器中通入0.5mol N2和1.5mol H2,乙容器中通入1mol N2和3molH2,后者反应放出的热量为前者的两倍.
| T/℃ | 30 | 40 | 50 |
| 生成NH3量/(10-6 mol) | 4.8 | 5.9 | 6.0 |
(1)该反应的平衡常数表达式为$\frac{[N{H}_{3}]^{2}×[{O}_{2}]^{\frac{3}{2}}}{[{N}_{2}]×[{H}_{2}O]^{3}}$.
(2)已知在所给条件下投入1molN2和3molH2O(l),当反应达到平衡时消耗了35kJ的热量,并收集到0.4molNH3.则N2的平衡转化率为20%,该反应的热化学方程式可表示为N2(g)+3H2O(l)?2NH3(g)+$\frac{3}{2}$O2(g)△H=+175.0kJ•mol-1.
(3)与目前广泛应用的工业合成氨方法相比,该方法中固氮反应速率较慢,请提出可提高其反应速率同时增大NH3生成量的措施升高温度、增大氮气浓度.(列出两种即可)
(4)工业合成氨的热化学方程式为N2(g)+3H2(g)?2NH3(g),△H=-92.4kJ•mol-1.在某体积为10L的恒温恒容密闭容器中加入2mol N2和4mol H2,2min后反应达到平衡时容器内的压强是起始压强的2/3.求:
①2min内NH3的反应速率υ(NH3)=0.1 mol/(L•min).
②下列有关该化学反应的说法正确的是B(填字母序号).
A.在恒温恒压条件下,向上述平衡体系中通入少量氩气,平衡不移动
B.在恒温恒容条件下,向上述平衡体系中通入少量氩气,平衡不移动
C.实际工业生产中为提高H2的转化率,通常通入过量的N2,且N2过量越多越好
D.当温度、体积相同且恒定不变时,向甲容器中通入0.5mol N2和1.5mol H2,乙容器中通入1mol N2和3molH2,后者反应放出的热量为前者的两倍.
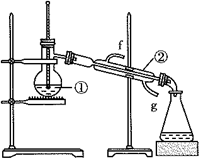 如图为蒸馏实验装置:
如图为蒸馏实验装置: