题目内容
2.短周期元素A、B可形成A3B2型化合物,若B的原子序数为 b,则A的原子序数不可能为( )| A. | b+1 | B. | b+5 | C. | b+4 | D. | b-11 |
分析 短周期元素A、B可形成A3B2型化合物,A的化合价为+2价,B为-3价,A可为Be、Mg,B可为N、P等元素,以此解答该题.
解答 解:短周期元素A、B可形成A3B2型化合物,A的化合价为+2价,B为-3价,A可为Be、Mg,原子序数分别为4、12,B可为N、P等元素,原子序数分别为7、15,
形成的化合物可能为Be3N2、Mg3N2、Be3P2、Mg3P2,则若B的原子序数为 b,则A的原子序数可能为b+5、b-11、b-3,
故选A.
点评 本题考查学生利用化合价与化学式及核电荷数的关系,学生应熟悉常见的化合物中的元素的化合价及元素的核电荷数,能利用举例的方法或价序原则来分析解答.

练习册系列答案
 一本好题口算题卡系列答案
一本好题口算题卡系列答案
相关题目
13.①氧化钠②氢氧化钠③过氧化钠 ④亚硫酸钠,1mol上述固体物质长期放置于空气中,下列说法正确的是( )
| A. | 上述物质都有发生了氧化还原反应 | |
| B. | 过氧化钠在反应中转移了2 mol电子 | |
| C. | 质量增加的情况是①>③>④>② | |
| D. | 质量增加的情况是②>①>③>① |
10.设NA为阿伏伽德罗常数,下列说法不正确的是( )
| A. | 含1molFeCl3的饱和溶液最多可形成胶体粒子数为NA | |
| B. | 4.6gNa与稀盐酸反应,转移电子数一定为0.2NA | |
| C. | 10.6gNa2CO3晶体中含CO32-数目为0.1NA | |
| D. | 常温下,22gCO2含碳氧双键数目为NA |
17.下列各组原子中,第一电离能前者大于后者的是( )
| A. | S和P | B. | Mg和Al | C. | Na和Mg | D. | Ne和He |
7.白藜芦醇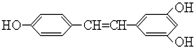 广泛存在于食物(例如桑椹、花生、尤其是葡萄)中,它可能具有搞癌性.能够跟1摩尔该化合物起反应的Br2或H2的最大用量分别是( )
广泛存在于食物(例如桑椹、花生、尤其是葡萄)中,它可能具有搞癌性.能够跟1摩尔该化合物起反应的Br2或H2的最大用量分别是( )
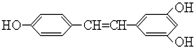 广泛存在于食物(例如桑椹、花生、尤其是葡萄)中,它可能具有搞癌性.能够跟1摩尔该化合物起反应的Br2或H2的最大用量分别是( )
广泛存在于食物(例如桑椹、花生、尤其是葡萄)中,它可能具有搞癌性.能够跟1摩尔该化合物起反应的Br2或H2的最大用量分别是( )| A. | 1 mol 1 mol | B. | 3.5 mol 7 mol | C. | 3.5 mol 6 mol | D. | 6 mol 7 mol |
11.下列有关碳和碳的化合物的说法中,错误的是( )
| A. | 金刚石和石墨物理性质不同,是因为它们的碳原子排列方式不同 | |
| B. | 一氧化碳、二氧化碳、葡萄糖都属于有机物 | |
| C. | 木炭、一氧化碳在一定条件下都能与氧化铜反应 | |
| D. | 大气中二氧化碳的消耗途径主要是绿色植物的光合作用 |
12.下列微粒中不具有正四面体结构的是( )
| A. | NH4+ | B. | 金刚石 | C. | 甲烷 | D. | H2O |