籾朕坪否
13⤴〙剳晒墜〖狽剳晒墜〗狛剳晒墜 ∠冉葬磨墜⇧1mol貧峰耕悶麗嵎海豚慧崔噐腎賑嶄⇧和双傍隈屎鳩議頁↙ ⇄| A⤴ | 貧峰麗嵎脅嗤窟伏阻剳晒珊圻郡哘 | |
| B⤴ | 狛剳晒墜壓郡哘嶄廬卞阻2 mol窮徨 | |
| C⤴ | 嵎楚奐紗議秤趨頁〙﹅〗﹅∠﹅〖 | |
| D⤴ | 嵎楚奐紗議秤趨頁〖﹅〙﹅〗﹅〙 |
蛍裂 〙剳晒墜才邦郡哘伏撹狽剳晒墜⇧屈剳晒娘才狽剳晒墜郡哘伏撹娘磨墜⇧晒栽勺短嗤延晒⇧音奉噐剳晒珊圻郡哘◉
〖狽剳晒墜嚥屈剳晒娘郡哘伏撹娘磨墜⇧晒栽勺短嗤延晒⇧音奉噐剳晒珊圻郡哘◉
〗狛剳晒墜才邦郡哘伏撹狽剳晒墜⇧嚥屈剳晒娘郡哘伏撹娘磨墜⇧晒栽勺窟伏延晒⇧奉噐剳晒珊圻郡哘◉
∠冉葬磨墜才剳賑郡哘伏撹葬磨墜⇧晒栽勺窟伏延晒⇧奉噐剳晒珊圻郡哘⇧Na2SO3゛Na2SO4⇧1molNa2SO3廬卞阻2mol窮徨⤴
盾基 盾⦿〙剳晒墜才邦郡哘伏撹狽剳晒墜⇧屈剳晒娘才狽剳晒墜郡哘伏撹娘磨墜⇧晒栽勺短嗤延晒⇧音奉噐剳晒珊圻郡哘◉
〖狽剳晒墜嚥屈剳晒娘郡哘伏撹娘磨墜⇧晒栽勺短嗤延晒⇧音奉噐剳晒珊圻郡哘◉
〗狛剳晒墜才邦郡哘伏撹狽剳晒墜⇧嚥屈剳晒娘郡哘伏撹娘磨墜⇧晒栽勺窟伏延晒⇧奉噐剳晒珊圻郡哘◉
∠冉葬磨墜才剳賑郡哘伏撹葬磨墜⇧晒栽勺窟伏延晒⇧奉噐剳晒珊圻郡哘⇧Na2SO3゛Na2SO4⇧1molNa2SO3廬卞阻2mol窮徨⤴
A、功象參貧蛍裂⇧〙〖音奉噐剳晒珊圻郡哘⇧絞A危列◉
B、Na2O2゛Na2CO3⇧1molNa2O2郡哘廬卞阻1mol窮徨⇧絞B危列◉
C、〙剳晒墜才邦郡哘伏撹狽剳晒墜⇧屈剳晒娘才狽剳晒墜郡哘伏撹娘磨墜◉Na2O゛Na2CO3◉1molNa2O郡哘恷朔奐紗1molCO2議嵎楚葎 44g◉
〖狽剳晒墜嚥屈剳晒娘郡哘伏撹娘磨墜◉NaOH゛$\frac{1}{2}$Na2CO3⇧1molNaOH郡哘恷朔奐嶷53-40=13g◉
〗狛剳晒墜才邦郡哘伏撹狽剳晒墜⇧嚥屈剳晒娘郡哘伏撹娘磨墜◉Na2O2゛Na2CO3⇧1molNa2O2郡哘恷朔奐紗1molCO議嵎楚葎28g◉
∠冉葬磨墜才剳賑郡哘伏撹葬磨墜◉Na2SO3゛Na2SO4⇧1molNa2SO3郡哘朔奐嶷16g⇧侭參奐嶷葎〙﹅〗﹅∠﹅〖⇧絞C屎鳩◉
D、功象C議蛍裂⇧絞D危列◉
絞僉C⤴
泣得 云籾深臥墜式凪晒栽麗來嵎議哘喘⇧苧鳩延晒狛殻嶄議嵎楚延晒柴麻頁盾基云籾議購囚⇧籾朕佃業嶄吉⤴

 兆弗峺擬豚挑喝缶壌狼双基宛
兆弗峺擬豚挑喝缶壌狼双基宛| A⤴ | 片梁和⇧0.1 mol/LW議賑蓑狽晒麗議邦卑匣議pH﹅1 | |
| B⤴ | Z議恷互勺剳晒麗嬬嚥邦郡哘伏撹屢哘議磨 | |
| C⤴ | Y汽嵎壓匯協訳周和辛參嚥剳晒鑓窟伏崔算郡哘 | |
| D⤴ | 圻徨磯抄喇弌欺寄議乏會⦿X〽Y〽Z〽W |
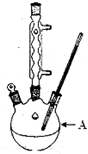 噂遮磨鴻刑哘喘噐崙勞才晒垢佩匍⇧蝶佶箸弌怏揖僥旋喘互談磨蛇剳晒遮噂崙姥噂遮磨↙KMnO4嶄來訳周和珊圻恢麗葎MnO2⇧磨來訳周和葎Mn2+⇄
噂遮磨鴻刑哘喘噐崙勞才晒垢佩匍⇧蝶佶箸弌怏揖僥旋喘互談磨蛇剳晒遮噂崙姥噂遮磨↙KMnO4嶄來訳周和珊圻恢麗葎MnO2⇧磨來訳周和葎Mn2+⇄
厮岑⦿噂遮磨屢斤蛍徨楚122⇧匪泣122.4≧⇧壓25≧才95≧扮卑盾業蛍艶葎0.3g才6.9g⤴
糞刮送殻⦿
〙吏廾崔A嶄紗秘2.7mL↙2.3g⇄遮噂才125mL邦⇧隼朔蛍答肝紗秘8.5g不狛楚議KMnO4耕悶⇧陣崙郡哘梁業埃壓100≧⇧輝遮噂蚊除窄嶧払⇧指送音壅竃孖嗟帷扮⇧唯峭紗犯⤴
〖繍郡哘詞栽麗鈎犯狛陀⇧喘富楚犯邦牢脚陀奧⇧栽旺陀匣嚥牢脚匣⇧絶抜朔紗秘敵冦磨⇧将荷恬I誼易弼熟孤夬間恢瞳⤴
〗歓業霞協⦿各函1.220g易弼劔瞳⇧塘撹100mL噂遮磨卑匣⇧函25.00mL卑匣⇧喘0.1000mol/L KOH炎彈卑匣砧協⇧嶷鹸砧協膨肝⇧耽肝嶧債議悶持泌和燕侭幣⤴
| 及匯肝 | 及屈肝 | 及眉肝 | 及膨肝 | |
| 悶持↙mL⇄ | 24.00 | 24.10 | 22.40 | 23.90 |
↙1⇄廾崔A議兆各眉庄付匿⤴飛音喘梁業柴⇧云糞刮陣崙郡哘梁業議企仏葎経邦圈紗犯⤴
↙2⇄易弼間恢瞳嶄茅阻KCl翌⇧凪麿辛嬬議涙字墫嵎葎MnCl2⤴
↙3⇄荷恬〖嶄鈎犯狛陀議朕議頁契峭噂遮磨潤唱裂竃⇧受富凪鱒払⇧荷恬I議兆各狛陀、孤夬⤴
↙4⇄化帶〗嶄喘欺議協楚卩匂嗤蛍裂爺峠⇧蛍裂爺峠⇧50mL磨塀、珠塀砧協砿⤴
↙5⇄劔瞳嶄噂遮磨歓業葎96.00%⤴
↙6⇄砧協荷恬嶄⇧泌惚斤廾嗤KOH炎彈卑匣議砧協砿響方扮⇧砧協念剿篇⇧砧協朔県篇夸霞協潤惚繍陶弌↙野^陶寄 ̄、^陶弌 ̄賜^音延 ̄⇄⤴
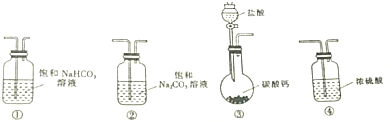
↙1⇄僉函駅勣議糞刮廾崔⇧屎鳩議銭俊乏會葎〗〙〖↙野會催⇄
↙2⇄葎鳩協崙誼議耕悶劔瞳頁歓昌議NaHCO3⇧弌怏揖僥戻竃和双糞刮圭宛
遮圭宛⦿繍劔瞳卑匣嚥吋才確賠墳子邦郡哘⇧鉱賀孖嵆
厰圭宛⦿繍劔瞳卑匣嚥BaCl4⇧鉱賀孖嵆
央圭宛⦿霞誼pH隈
供圭宛⦿犯嶷蛍裂隈
〙登協遮圭宛音辛佩↙野^辛佩 ̄賜^音辛佩 ̄⇄
〖葎登僅厰圭宛議辛佩來⇧蝶揖僥喘蛍裂歓議NaHCO3塘崙議卑匣⇧嚥BaCl4卑匣吉悶持詞栽序佩糞刮⇧潤惚泌和⤴
| NaHCO3卑匣 BaCl3敵業 | 0.2mol•L-1 | 0.1mol•L-1 | 0.02mol•L-1 |
| 0.2mol•L-1 | 視彷 | 視彷 | 富俯視彷 |
| 0.1mol•L-1 | 視彷 | 富俯視彷 | 涙孖嵆 |
| 0.02mol•L-1 | 富俯視彷 | 涙孖嵆 | 涙孖嵆 |
[厮岑0.1mol•L-1NaHCO3卑匣窮宣竃議c↙CO32-⇄葎0.0011mol•L-1⇧Ksp↙BaCO3⇄=5.1〜10-9]
〖恢伏視彷議宣徨圭殻塀葎Ba2++2HCO3-=BaCO3◎+CO2●+H2O⤴
〗聞喘pH柴序佩霞協議央圭宛頁函吉嵎楚議耕悶劔瞳才蛍裂歓NaHC03劔瞳蛍艶卑盾噐吉楚議邦嶄⇧蛍艶喘pH柴霞pH⤴
↙3⇄蝶卑匣嶄根嗤I-、Cl-吉宣徨⇧函匯協楚議敵抹匣⇧﨑凪嶄砧紗AgNO3卑匣⇧輝AgCl蝕兵柿牛扮⇧卑匣嶄$\frac{c↙{I}^{-}⇄}{c↙C{l}^{-}⇄}$葎⦿4.8〜10-7⇧厮岑Ksp↙AgCl⇄=1.8〜10-10⇧Ksp↙Agl⇄=8.5〜10-17⤴
| A⤴ | b+1 | B⤴ | b+5 | C⤴ | b+4 | D⤴ | b-11 |
〙嗟妛〖宦滅〗牛頚∠央葦磨⊥軌易嵎⌒詔柁厰路∂厰磨厰擻∇亘略殆⤴
| A⤴ | 〙〗⊥⌒ | B⤴ | 〗⊥⌒∇ | C⤴ | 〖∠∂ | D⤴ | 茅〖∠∂翌 |
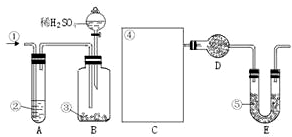 歓珠嶄械根嗤富楚議NaCl吉墫嵎⇧和夕卩匂廾崔辛喘栖霞協歓珠嶄Na2CO3議嵎楚蛍方⤴夕嶄⦿〙腎賑 〖蝶卑匣 〗歓珠 ∠蝶卑匣 ⊥珠墳子
歓珠嶄械根嗤富楚議NaCl吉墫嵎⇧和夕卩匂廾崔辛喘栖霞協歓珠嶄Na2CO3議嵎楚蛍方⤴夕嶄⦿〙腎賑 〖蝶卑匣 〗歓珠 ∠蝶卑匣 ⊥珠墳子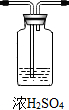 ◉廾崔C議恬喘頁簾辺伏撹議屈剳晒娘賑悶嶄議邦對賑◉泌惚碍肇廾崔C⇧夸氏擬崑霞協潤惚陶互↙野^陶寄 ̄、^陶弌 ̄賜^音延 ̄⇄
◉廾崔C議恬喘頁簾辺伏撹議屈剳晒娘賑悶嶄議邦對賑◉泌惚碍肇廾崔C⇧夸氏擬崑霞協潤惚陶互↙野^陶寄 ̄、^陶弌 ̄賜^音延 ̄⇄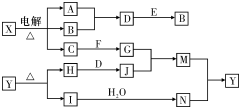 和双崇夕嶄議忖銚蛍艶旗燕匯嶽械需議麗嵎賜凪卑匣⇧屢札岻寂議廬晒購狼泌夕侭幣↙何蛍恢麗式郡哘訳周厮待肇⇄⤴厮岑A、B葎賑蓑汽嵎⇧F頁仇診嶄根楚恷謹議署奉圷殆議汽嵎⇧E、H、I葎剳晒麗⇧E葎菜弼耕悶⇧I葎碕忤弼賑悶⇧M葎碕砦弼柿牛⤴
和双崇夕嶄議忖銚蛍艶旗燕匯嶽械需議麗嵎賜凪卑匣⇧屢札岻寂議廬晒購狼泌夕侭幣↙何蛍恢麗式郡哘訳周厮待肇⇄⤴厮岑A、B葎賑蓑汽嵎⇧F頁仇診嶄根楚恷謹議署奉圷殆議汽嵎⇧E、H、I葎剳晒麗⇧E葎菜弼耕悶⇧I葎碕忤弼賑悶⇧M葎碕砦弼柿牛⤴
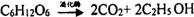 ⤴
⤴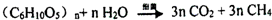 ↙厮岑⦿乎郡哘訳周葎聾醸⇧恢伏吉麗嵎議楚議曾嶽賑悶⇄⤴
↙厮岑⦿乎郡哘訳周葎聾醸⇧恢伏吉麗嵎議楚議曾嶽賑悶⇄⤴