ΧβΡΩΡΎ»ί
”–XΓΔYΓΔZΓΔWΥΡ÷÷‘Ύ÷–―ß―ßΙΐΒΡΙΧΧεΜ·ΚœΈοΘ§ Β―ιœ÷œσ»γœ¬ΘΚ
ΔΌXΓΔYΓΔZΓΔWΒΡ―φ…ΪΖ¥”ΠΨυΈΣΜΤ…ΪΘ°
ΔΎ‘ΎZΓΔW÷–Φ”»κœΓ―ΈΥαΘ§Ψυ”–Έό…ΪΓΔΈόΤχΈΕΒΡΤχΧεΖ≈≥ωΘ°
ΔέYΓΔZΓΔWΖ÷±π”κ ΝΩΒΡBaΘ®OHΘ©2≈®»ή“ΚΖ¥”ΠΘ§Ψυ”–ΑΉ…Ϊ≥ΝΒμ…ζ≥…ΘΜ‘ΌΦ”»κΙΐΝΩ―ΈΥαΘ§”…ZΓΔW…ζ≥…ΒΡΑΉ…Ϊ≥ΝΒμΨυ»ήΫβΘ§”…Y…ζ≥…ΒΡΑΉ…Ϊ≥ΝΒμ≤Μ»ήΫβΘ°
Δή‘ΎœύΆ§ΧθΦΰœ¬Θ§ΫΪΉψΝΩΒΡYΒΡ»ή“ΚΖ÷±πΦ”ΒΫœύΆ§Έο÷ ΒΡΝΩ≈®Ε»ΓΔœύΆ§ΧεΜΐΒΡZΚΆWΒΡ»ή“Κ÷–Θ§ΕΦ”–Τχ≈ί≥ωœ÷Θ°Τδ÷–W»ή“Κ÷–Τχ≈ί≥ωœ÷ΫœΩλΘ°
ΔίX”κCO2Ζ¥”Π…ζ≥…ZΘ§Ά§ ±…ζ≥…Νμ“Μ÷÷ΤχΧεΘ§¥ΥΤχΧε”…ΒΊΩ«÷–Κ§ΝΩΉνΕύΒΡ‘ΣΥΊΉι≥…Θ°
ΗυΨί…œ ωœ÷œσΘ§ΜΊ¥πœ¬Ν–Έ ΧβΘΚ
Θ®1Θ©XΒΡΜ·―ß ΫΈΣ
Θ®2Θ©–¥≥ωœ¬Ν–”–ΙΊΖ¥”ΠΒΡΜ·―ßΖΫ≥Χ ΫΜράκΉ”ΖΫ≥Χ ΫΘ°
ΔΌZ+ ·Μ“Υ°Θ®άκΉ”ΖΫ≥Χ ΫΘ©
ΔΎX+CO2Θ®Μ·―ßΖΫ≥Χ ΫΘ©
ΔέW
Θ®Μ·―ßΖΫ≥Χ ΫΘ©
ΔΌXΓΔYΓΔZΓΔWΒΡ―φ…ΪΖ¥”ΠΨυΈΣΜΤ…ΪΘ°
ΔΎ‘ΎZΓΔW÷–Φ”»κœΓ―ΈΥαΘ§Ψυ”–Έό…ΪΓΔΈόΤχΈΕΒΡΤχΧεΖ≈≥ωΘ°
ΔέYΓΔZΓΔWΖ÷±π”κ ΝΩΒΡBaΘ®OHΘ©2≈®»ή“ΚΖ¥”ΠΘ§Ψυ”–ΑΉ…Ϊ≥ΝΒμ…ζ≥…ΘΜ‘ΌΦ”»κΙΐΝΩ―ΈΥαΘ§”…ZΓΔW…ζ≥…ΒΡΑΉ…Ϊ≥ΝΒμΨυ»ήΫβΘ§”…Y…ζ≥…ΒΡΑΉ…Ϊ≥ΝΒμ≤Μ»ήΫβΘ°
Δή‘ΎœύΆ§ΧθΦΰœ¬Θ§ΫΪΉψΝΩΒΡYΒΡ»ή“ΚΖ÷±πΦ”ΒΫœύΆ§Έο÷ ΒΡΝΩ≈®Ε»ΓΔœύΆ§ΧεΜΐΒΡZΚΆWΒΡ»ή“Κ÷–Θ§ΕΦ”–Τχ≈ί≥ωœ÷Θ°Τδ÷–W»ή“Κ÷–Τχ≈ί≥ωœ÷ΫœΩλΘ°
ΔίX”κCO2Ζ¥”Π…ζ≥…ZΘ§Ά§ ±…ζ≥…Νμ“Μ÷÷ΤχΧεΘ§¥ΥΤχΧε”…ΒΊΩ«÷–Κ§ΝΩΉνΕύΒΡ‘ΣΥΊΉι≥…Θ°
ΗυΨί…œ ωœ÷œσΘ§ΜΊ¥πœ¬Ν–Έ ΧβΘΚ
Θ®1Θ©XΒΡΜ·―ß ΫΈΣ
Na2O2
Na2O2
Θ§YΒΡΜ·―ß ΫΈΣNaHSO4
NaHSO4
ΘΜΘ®2Θ©–¥≥ωœ¬Ν–”–ΙΊΖ¥”ΠΒΡΜ·―ßΖΫ≥Χ ΫΜράκΉ”ΖΫ≥Χ ΫΘ°
ΔΌZ+ ·Μ“Υ°Θ®άκΉ”ΖΫ≥Χ ΫΘ©
Ca2++CO32-®TCaCO3Γΐ
Ca2++CO32-®TCaCO3Γΐ
ΘΜΔΎX+CO2Θ®Μ·―ßΖΫ≥Χ ΫΘ©
2Na2O2+2CO2=2Na2CO3+O2
2Na2O2+2CO2=2Na2CO3+O2
ΘΜΔέW
| Γς |
2NaHCO3
Na2CO3+H2O+CO2Γϋ
| ||
2NaHCO3
Na2CO3+H2O+CO2Γϋ
Θ°
| ||
Ζ÷ΈωΘΚXΓΔYΓΔZΓΔWΈΣΥΡ÷÷ΙΧΧεΜ·ΚœΈοΘ§ Β―ιœ÷œσ»γœ¬ΘΚ
ΔΌXΓΔYΓΔZΓΔWΒΡ―φ…ΪΖ¥”ΠΨυΈΣΜΤ…ΪΘ§÷ΛΟςΚ§ΡΤ‘ΣΥΊΘΜ
ΔΎ‘ΎZΓΔW÷–Φ”»κœΓ―ΈΥαΘ§Ψυ”–Έό…ΪΓΔΈόΤχΈΕΒΡΤχΧεΖ≈≥ωΘ§Ω…ΆΤΕœΈΣΧΦΥαΡΤΜρΧΦΥα«βΡΤΘΜ
ΔέYΓΔZΓΔWΖ÷±π”κ ΝΩΒΡBaΘ®OHΘ©2≈®»ή“ΚΖ¥”ΠΘ§Ψυ”–ΑΉ…Ϊ≥ΝΒμ…ζ≥…ΘΜ‘ΌΦ”»κΙΐΝΩ―ΈΥαΘ§”…ZΓΔW…ζ≥…ΒΡΑΉ…Ϊ≥ΝΒμΨυ»ήΫβΘ§”…Y…ζ≥…ΒΡΑΉ…Ϊ≥ΝΒμ≤Μ»ήΫβΘ§÷ΛΟςZWΈΣΧΦΥαΡΤΚΆΧΦΥα«βΡΤΘ§YΩ…ΡήΈΣΝρΥαΡΤΜρΝρΥα«βΡΤΘΜ
Δή‘ΎœύΆ§ΧθΦΰœ¬Θ§ΫΪΉψΝΩΒΡYΒΡ»ή“ΚΖ÷±πΦ”ΒΫœύΆ§Έο÷ ΒΡΝΩ≈®Ε»ΓΔœύΆ§ΧεΜΐΒΡZΚΆWΒΡ»ή“Κ÷–Θ§ΕΦ”–Τχ≈ί≥ωœ÷Θ°Τδ÷–W»ή“Κ÷–Τχ≈ί≥ωœ÷ΫœΩλΘ§ΥΒΟςY“ΜΕ®ΈΣNaHSO4ΘΜ
ΔίX”κCO2Ζ¥”Π…ζ≥…ZΘ§ΆΤΕœZΈΣNa2CO3Θ§WΈΣNaHCO3Θ§Ά§ ±…ζ≥…Νμ“Μ÷÷ΤχΧεΘ§¥ΥΤχΧε”…ΒΊΩ«÷–Κ§ΝΩΉνΕύΒΡ‘ΣΥΊΉι≥…Θ§≈–ΕœΈΣO2ΘΜΥυ“‘XΈΣNa2O2ΘΜ
Ήέ…œΥυ ωΘΚXΈΣNa2O2ΓΔYΈΣNaHSO4ΓΔZΈΣNa2CO3ΓΔWΈΣNaHCO3Θ°
ΔΌXΓΔYΓΔZΓΔWΒΡ―φ…ΪΖ¥”ΠΨυΈΣΜΤ…ΪΘ§÷ΛΟςΚ§ΡΤ‘ΣΥΊΘΜ
ΔΎ‘ΎZΓΔW÷–Φ”»κœΓ―ΈΥαΘ§Ψυ”–Έό…ΪΓΔΈόΤχΈΕΒΡΤχΧεΖ≈≥ωΘ§Ω…ΆΤΕœΈΣΧΦΥαΡΤΜρΧΦΥα«βΡΤΘΜ
ΔέYΓΔZΓΔWΖ÷±π”κ ΝΩΒΡBaΘ®OHΘ©2≈®»ή“ΚΖ¥”ΠΘ§Ψυ”–ΑΉ…Ϊ≥ΝΒμ…ζ≥…ΘΜ‘ΌΦ”»κΙΐΝΩ―ΈΥαΘ§”…ZΓΔW…ζ≥…ΒΡΑΉ…Ϊ≥ΝΒμΨυ»ήΫβΘ§”…Y…ζ≥…ΒΡΑΉ…Ϊ≥ΝΒμ≤Μ»ήΫβΘ§÷ΛΟςZWΈΣΧΦΥαΡΤΚΆΧΦΥα«βΡΤΘ§YΩ…ΡήΈΣΝρΥαΡΤΜρΝρΥα«βΡΤΘΜ
Δή‘ΎœύΆ§ΧθΦΰœ¬Θ§ΫΪΉψΝΩΒΡYΒΡ»ή“ΚΖ÷±πΦ”ΒΫœύΆ§Έο÷ ΒΡΝΩ≈®Ε»ΓΔœύΆ§ΧεΜΐΒΡZΚΆWΒΡ»ή“Κ÷–Θ§ΕΦ”–Τχ≈ί≥ωœ÷Θ°Τδ÷–W»ή“Κ÷–Τχ≈ί≥ωœ÷ΫœΩλΘ§ΥΒΟςY“ΜΕ®ΈΣNaHSO4ΘΜ
ΔίX”κCO2Ζ¥”Π…ζ≥…ZΘ§ΆΤΕœZΈΣNa2CO3Θ§WΈΣNaHCO3Θ§Ά§ ±…ζ≥…Νμ“Μ÷÷ΤχΧεΘ§¥ΥΤχΧε”…ΒΊΩ«÷–Κ§ΝΩΉνΕύΒΡ‘ΣΥΊΉι≥…Θ§≈–ΕœΈΣO2ΘΜΥυ“‘XΈΣNa2O2ΘΜ
Ήέ…œΥυ ωΘΚXΈΣNa2O2ΓΔYΈΣNaHSO4ΓΔZΈΣNa2CO3ΓΔWΈΣNaHCO3Θ°
Ϋβ¥πΘΚΫβΘΚ”…ΔΌXΓΔYΓΔZΓΔWΒΡ―φ…ΪΖ¥”ΠΨυΈΣΜΤ…ΪΘ§÷ΛΟςΚ§ΡΤ‘ΣΥΊΘΜ
ΔΎ‘ΎZΓΔW÷–Φ”»κœΓ―ΈΥαΘ§Ψυ”–Έό…ΪΓΔΈόΤχΈΕΒΡΤχΧεΖ≈≥ωΘ§Ω…ΆΤΕœΈΣΧΦΥαΡΤΜρΧΦΥα«βΡΤΘΜ
ΔέYΓΔZΓΔWΖ÷±π”κ ΝΩΒΡBaΘ®OHΘ©2≈®»ή“ΚΖ¥”ΠΘ§Ψυ”–ΑΉ…Ϊ≥ΝΒμ…ζ≥…ΘΜ‘ΌΦ”»κΙΐΝΩ―ΈΥαΘ§”…ZΓΔW…ζ≥…ΒΡΑΉ…Ϊ≥ΝΒμΨυ»ήΫβΘ§”…Y…ζ≥…ΒΡΑΉ…Ϊ≥ΝΒμ≤Μ»ήΫβΘ§÷ΛΟςZWΈΣΧΦΥαΡΤΚΆΧΦΥα«βΡΤΘ§YΩ…ΡήΈΣΝρΥαΡΤΜρΝρΥα«βΡΤΘΜ
Δή‘ΎœύΆ§ΧθΦΰœ¬Θ§ΫΪΉψΝΩΒΡYΒΡ»ή“ΚΖ÷±πΦ”ΒΫœύΆ§Έο÷ ΒΡΝΩ≈®Ε»ΓΔœύΆ§ΧεΜΐΒΡZΚΆWΒΡ»ή“Κ÷–Θ§ΕΦ”–Τχ≈ί≥ωœ÷Θ°Τδ÷–W»ή“Κ÷–Τχ≈ί≥ωœ÷ΫœΩλΘ§ΥΒΟςY“ΜΕ®ΈΣNaHSO4ΘΜ
ΔίX”κCO2Ζ¥”Π…ζ≥…ZΘ§ΆΤΕœZΈΣNa2CO3Θ§WΈΣNaHCO3Θ§Ά§ ±…ζ≥…Νμ“Μ÷÷ΤχΧεΘ§¥ΥΤχΧε”…ΒΊΩ«÷–Κ§ΝΩΉνΕύΒΡ‘ΣΥΊΉι≥…Θ§≈–ΕœΈΣO2ΘΜΥυ“‘XΈΣNa2O2ΘΜ
Ήέ…œΥυ ωΘΚXΈΣNa2O2ΓΔYΈΣNaHSO4ΓΔZΈΣNa2CO3ΓΔWΈΣNaHCO3ΘΜ
Θ®1Θ©“άΨίΖ÷Έω≈–ΕœXΒΡΜ·―ß ΫΈΣNa2O2Θ§YΒΡΜ·―ß ΫΈΣNaHSO4Θ§Ι ¥πΑΗΈΣΘΚNa2O2ΘΜNaHSO4ΘΜ
Θ®2Θ©ΔΌZΘ®Na2CO3Θ©+ ·Μ“Υ°Ζ¥”ΠΒΡάκΉ”ΖΫ≥Χ ΫΘΚCa2++CO32-®TCaCO3ΓΐΘ§Ι ¥πΑΗΈΣΘΚCa2++CO32-®TCaCO3ΓΐΘΜ
ΔΎXΘ®Na2O2Θ©+CO2Μ·Ζ¥”ΠΒΡ―ßΖΫ≥Χ ΫΘΚ2Na2O2+2CO2=2Na2CO3+O2Θ§Ι ¥πΑΗΈΣΘΚ2Na2O2+2CO2=2Na2CO3+O2ΘΜ
ΔέW
Ζ¥”ΠΒΡΜ·―ßΖΫ≥Χ ΫΘΚ2NaHCO3
Na2CO3+H2O+CO2ΓϋΘ§Ι ¥πΑΗΈΣΘΚ2NaHCO3
Na2CO3+H2O+CO2ΓϋΘ°
ΔΎ‘ΎZΓΔW÷–Φ”»κœΓ―ΈΥαΘ§Ψυ”–Έό…ΪΓΔΈόΤχΈΕΒΡΤχΧεΖ≈≥ωΘ§Ω…ΆΤΕœΈΣΧΦΥαΡΤΜρΧΦΥα«βΡΤΘΜ
ΔέYΓΔZΓΔWΖ÷±π”κ ΝΩΒΡBaΘ®OHΘ©2≈®»ή“ΚΖ¥”ΠΘ§Ψυ”–ΑΉ…Ϊ≥ΝΒμ…ζ≥…ΘΜ‘ΌΦ”»κΙΐΝΩ―ΈΥαΘ§”…ZΓΔW…ζ≥…ΒΡΑΉ…Ϊ≥ΝΒμΨυ»ήΫβΘ§”…Y…ζ≥…ΒΡΑΉ…Ϊ≥ΝΒμ≤Μ»ήΫβΘ§÷ΛΟςZWΈΣΧΦΥαΡΤΚΆΧΦΥα«βΡΤΘ§YΩ…ΡήΈΣΝρΥαΡΤΜρΝρΥα«βΡΤΘΜ
Δή‘ΎœύΆ§ΧθΦΰœ¬Θ§ΫΪΉψΝΩΒΡYΒΡ»ή“ΚΖ÷±πΦ”ΒΫœύΆ§Έο÷ ΒΡΝΩ≈®Ε»ΓΔœύΆ§ΧεΜΐΒΡZΚΆWΒΡ»ή“Κ÷–Θ§ΕΦ”–Τχ≈ί≥ωœ÷Θ°Τδ÷–W»ή“Κ÷–Τχ≈ί≥ωœ÷ΫœΩλΘ§ΥΒΟςY“ΜΕ®ΈΣNaHSO4ΘΜ
ΔίX”κCO2Ζ¥”Π…ζ≥…ZΘ§ΆΤΕœZΈΣNa2CO3Θ§WΈΣNaHCO3Θ§Ά§ ±…ζ≥…Νμ“Μ÷÷ΤχΧεΘ§¥ΥΤχΧε”…ΒΊΩ«÷–Κ§ΝΩΉνΕύΒΡ‘ΣΥΊΉι≥…Θ§≈–ΕœΈΣO2ΘΜΥυ“‘XΈΣNa2O2ΘΜ
Ήέ…œΥυ ωΘΚXΈΣNa2O2ΓΔYΈΣNaHSO4ΓΔZΈΣNa2CO3ΓΔWΈΣNaHCO3ΘΜ
Θ®1Θ©“άΨίΖ÷Έω≈–ΕœXΒΡΜ·―ß ΫΈΣNa2O2Θ§YΒΡΜ·―ß ΫΈΣNaHSO4Θ§Ι ¥πΑΗΈΣΘΚNa2O2ΘΜNaHSO4ΘΜ
Θ®2Θ©ΔΌZΘ®Na2CO3Θ©+ ·Μ“Υ°Ζ¥”ΠΒΡάκΉ”ΖΫ≥Χ ΫΘΚCa2++CO32-®TCaCO3ΓΐΘ§Ι ¥πΑΗΈΣΘΚCa2++CO32-®TCaCO3ΓΐΘΜ
ΔΎXΘ®Na2O2Θ©+CO2Μ·Ζ¥”ΠΒΡ―ßΖΫ≥Χ ΫΘΚ2Na2O2+2CO2=2Na2CO3+O2Θ§Ι ¥πΑΗΈΣΘΚ2Na2O2+2CO2=2Na2CO3+O2ΘΜ
ΔέW
| Γς |
| ||
| ||
ΒψΤάΘΚ±ΨΧβΩΦ≤ιΝΥΈο÷ ΉΣΜ·ΙΊœΒΒΡΖ÷Έω≈–ΕœΘ§Έο÷ –‘÷ ΒΡ”Π”ΟΘ§÷ς“ΣΩΦ≤ιΡΤΦΑΤδΜ·ΚœΈοΒΡ–‘÷ ”Π”ΟΘ§άκΉ”ΖΫ≥Χ ΫΓΔΜ·―ßΖΫ≥Χ ΫΒΡ ι–¥ΖΫΖ®Θ§Ζ¥”Πœ÷œσΚΆΈο÷ –‘÷ «ΫβΧβΙΊΦϋΘ°

ΝΖœΑ≤αœΒΝ–¥πΑΗ
 ΧλΧλœρ…œ“Μ±ΨΚΟΨμœΒΝ–¥πΑΗ
ΧλΧλœρ…œ“Μ±ΨΚΟΨμœΒΝ–¥πΑΗ –Γ―ß…ζ10Ζ÷÷””Π”ΟΧβœΒΝ–¥πΑΗ
–Γ―ß…ζ10Ζ÷÷””Π”ΟΧβœΒΝ–¥πΑΗ
œύΙΊΧβΡΩ


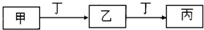
 ”–XΓΔYΓΔZΓΔWΥΡ÷÷ΕΧ÷ήΤΎ‘ΣΥΊΘ§‘≠Ή”–ρ ΐ“ά¥Έ‘ω¥σΘ°XΒΡ―τάκΉ”ΨΆ «“ΜΗω÷ Ή”Θ°ZΓΔW‘Ύ÷ήΤΎ±μΡΎ¥Π”ΎΆ§“Μ÷ήΤΎœύΝΎΈΜ÷ΟΘ°ΥϋΟ«ΒΡΒΞ÷ ‘ΎΆ®≥ΘΉ¥Ωωœ¬ΨυΈΣΈό…ΪΤχΧεΘ°Y‘≠Ή”ΒΡΉνΆβ≤ψΒγΉ” ΐ «¥ΈΆβ≤ψΒγΉ” ΐΒΡ2±ΕΘ°«κΜΊ¥πΘΚ
”–XΓΔYΓΔZΓΔWΥΡ÷÷ΕΧ÷ήΤΎ‘ΣΥΊΘ§‘≠Ή”–ρ ΐ“ά¥Έ‘ω¥σΘ°XΒΡ―τάκΉ”ΨΆ «“ΜΗω÷ Ή”Θ°ZΓΔW‘Ύ÷ήΤΎ±μΡΎ¥Π”ΎΆ§“Μ÷ήΤΎœύΝΎΈΜ÷ΟΘ°ΥϋΟ«ΒΡΒΞ÷ ‘ΎΆ®≥ΘΉ¥Ωωœ¬ΨυΈΣΈό…ΪΤχΧεΘ°Y‘≠Ή”ΒΡΉνΆβ≤ψΒγΉ” ΐ «¥ΈΆβ≤ψΒγΉ” ΐΒΡ2±ΕΘ°«κΜΊ¥πΘΚ