题目内容
4.填写下列空白.(1)表示含有17个质子、20个中子的原子的化学符号是3717Cl.
(2)第二周期ⅤA族元素的最高价氧化物的水化物的化学式为HNO3.
(3)原电池的本质是氧化还原反应.
(4)与Na+具有相同电子数的分子有H2O、CH4(写分子式,只写出两种).
(5)在①${\;}_{6}^{12}$C ②${\;}_{19}^{40}$K ③${\;}_{1}^{2}$H ④${\;}_{6}^{13}$C ⑤${\;}_{20}^{40}$Ca ⑥${\;}_{6}^{14}$C ⑦${\;}_{1}^{1}$H几种符号中,有7种核素,有4种元素;①、④、⑥互称为同位素.
(6)水分子中,共有2对共用电子.
(7)从能量角度看,断开化学键要吸收能量,形成化学键要放出能量,所有的燃烧反应都会放出能量.
分析 (1)含有17个质子、20个中子的原子为氯原子,质量数为37,据此答题;
(2)第二周期ⅤA族为氮元素,最高价为+5价,据此写最高价氧化物的水化物的化学式;
(3)原电池反应的本质是负极发生氧化反应,正极发生还原反应,电子由负极沿导线流向正极,从而实现将化学能转化为电能;
(4)Na+具有10个电子;
(5)核素是指具有一定数目质子和一定数目中子的一种原子;具有相同质子数的同一类原子是同种元素;具有相同质子数,不同中子数同一元素的不同原子互为同位素;
(6)O为-2价;
(7)断键吸收能量,成键放出能量,燃烧反应是指:混合物中的可燃成分急剧与氧反应形成火焰放出大量的热和强烈的光的过程;
解答 解:(1)含有17个质子、20个中子的原子为氯原子,质量数为37,原子的化学符号是3717Cl,
故答案为:3717Cl;
(2)第二周期ⅤA族为氮元素,最高价为+5价,最高价氧化物的水化物的化学式为HNO3,故答案为:HNO3;
(3)原电池反应的本质是自发的氧化还原反应,负极发生氧化反应,正极发生还原反应,故答案为:氧化还原反应;
(4)Na+具有10个电子,具有相同电子数的分子有Ne、HF、NH3、H2O、CH4,故答案为:H2O;CH4;
(5)核素是指具有一定数目的质子和一定数目的中子的一种原子,属于原子的有①${\;}_{6}^{12}$C ②${\;}_{19}^{40}$K ③${\;}_{1}^{2}$H ④${\;}_{6}^{13}$C ⑤${\;}_{20}^{40}$Ca ⑥${\;}_{6}^{14}$C ⑦${\;}_{1}^{1}$H,它们都表示核素,即共有7种核素;具有相同质子数的同一类原子是同种元素,有C、K、H、Ca4种元素;质子数相同而中子数不同的同一元素的不同原子互称同位素,在7种微粒中,①${\;}_{6}^{12}$C ④${\;}_{6}^{13}$C ⑥${\;}_{6}^{14}$C质子数都是6,而中子数分别为6、7、和8,即互为同位素,故答案为:7;4;同位素;
(6)O为-2价,H为+1价,水分子中,共有2对共用电子,故答案为:2;
(7)断键吸收能量,成键放出能量,燃烧反应是指:混合物中的可燃成分急剧与氧反应形成火焰放出大量的热和强烈的光的过程,是放热反应,故答案为:吸收;放出;放出.
点评 本题主要考查了原子结构、元素周期律、化学键等知识点,涉及面较广,难度不大,答题时注意基础知识掌握.

 阅读快车系列答案
阅读快车系列答案| A. | 0.1mol/L NaHCO3溶液与0.1mol/L NaOH溶液等体积混合,所得溶液:c(Na+)>c(CO32-)>c(HCO3- )>c(OH-) | |
| B. | pH相等的①NH4Cl ②(NH4)2SO4 ③NH4HSO4溶液中,c(NH4+)大小顺序:①=②>③ | |
| C. | 室温下,pH=2的盐酸与pH=12的氨水等体积混合,所得溶液中:c(Cl-)>c(H+)>c(NH4+ )>c(OH-) | |
| D. | 0.2mol•L-1CH3COOH溶液与0.1mol•L-1NaOH溶液等体积混合:2c(H+)-2c(OH-)═C(CH3COO-)+C(CH3COOH) |
 如果将前18号元素按原子序数递增的顺序排列,可形成如图所示的“蜗牛”形状,图中每个“•”代表一种元素,其中①点代表氢元素.下列说法不正确的是( )
如果将前18号元素按原子序数递增的顺序排列,可形成如图所示的“蜗牛”形状,图中每个“•”代表一种元素,其中①点代表氢元素.下列说法不正确的是( )| A. | 最简单气态氢化物的稳定性③比⑦小 | |
| B. | ①与④能形成原子个数比为1:1的化合物 | |
| C. | ⑤和⑥的最高价氧化物对应的水化物可以反应 | |
| D. | 原子半径②>③>④ |
| A. | 氯化钠溶液 | B. | 氯化钾晶体 | C. | 熔融KNO3 | D. | 氨水 |
| A. | 萃取、分液、过滤 | B. | 萃取、分液、蒸馏 | C. | 分液、蒸馏、过滤 | D. | 蒸馏、萃取、过滤 |
| A. | O2和O3互为同素异形体 | B. | 1H、2H和3H互为同位素 | ||
| C. | CH2═CH2和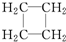 互为同系物 互为同系物 | D. | 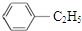 和 和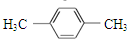 互为同分异构体 互为同分异构体 |
 A~G是前四周期除稀有气体之外原子序数依次增大的七种元素.A与其它元素既不同周期又不同族;B、C的价电子层中未成对电子数都是2;E核外的s、p能级的电子总数相等;F与E同周期且第一电离能比E小;G的+1价离子(G+)的各层电子全充满.请结合题目回答以下问题:
A~G是前四周期除稀有气体之外原子序数依次增大的七种元素.A与其它元素既不同周期又不同族;B、C的价电子层中未成对电子数都是2;E核外的s、p能级的电子总数相等;F与E同周期且第一电离能比E小;G的+1价离子(G+)的各层电子全充满.请结合题目回答以下问题: .
.