题目内容
9.下列试剂不能导电的是( )| A. | 氯化钠溶液 | B. | 氯化钾晶体 | C. | 熔融KNO3 | D. | 氨水 |
分析 含有自由移动离子或电子的物质能导电,金属单质、熔融态离子化合物、可溶性强电解质溶液等都能导电,据此分析解答.
解答 解:A.氯化钠溶液中含有自由移动离子,所以能导电,故A不选;
B.氯化钾晶体中不含自由移动离子或电子,所以不能导电,故B选;
C.熔融硝酸钾中含有自由移动离子,所以能导电,故C不选;
D.一水合氨是电解质,在水溶液中能电离出阴阳离子而使氨水导电,故D不选;
故选B.
点评 本题考查物质导电性,物质的导电性与是否含有自由移动离子或电子有关,注意不能根据是否是强电解质判断,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
19.从化学视角认识生产生活中的一些现象,其中错误的是( )
| A. | 打开汽水瓶盖时有大量气泡冒出,可用勒夏特列原理解释 | |
| B. | 用热的纯碱(Na2CO3)溶液容易洗去餐具上的油污 | |
| C. | 向牛奶中加入果汁会产生沉淀,这是因为酸碱发生了中和反应 | |
| D. | 用铁制自来水管与铜制水龙头连接使用时,连接处的铁水管锈蚀更快 |
20.某航空站安装了一台燃料电池,该电池可同时提供电和水蒸气.所用燃料为氢气,电解质为熔融的碳酸钾.已知该电池的总反应为2H2+O2═2H2O,正极反应为O2+2CO2+4e-═2CO3-,则下列推断正确的是( )
| A. | 负极反应为H2+2OH--2e-═2H2O | |
| B. | 放电时负极有CO2生成 | |
| C. | 该电池供应2 mol水蒸气,同时转移2 mol电子 | |
| D. | 该电池可在常温或高温时进行工作,对环境具有较强的适应性 |
17.1mol某烃最多能和2molHCl发生加成反应,生成1mol氯代烷,1mol此氯代烷能和8molCl2发生取代反应,生成只含碳元素和氯元素的氯代烷,该烃可能是( )
| A. | CH3CH=CH2 | B. | CH2=CHCH=CH2 | C. | CH3=CHCH3 | D. | CH3-C≡CH2-CH3 |
14.2015年2月28日,央视原记者柴静及其团队制作的视频《穹顶之下》引起了人们对环境保护的再思考,下列说法体现人与自然和谐相处的是( )
| A. | 将聚氯乙烯等塑料垃圾焚烧 | |
| B. | 推广矿物燃料脱硫技术以减少SO2等有害气体的排放 | |
| C. | 大力开采石油、煤、页岩气(主要成分为CH4)等化石燃料 | |
| D. | 电池使用后随意丢弃,无需处理 |
18.下图是元素周期表的一部分,针对表中的①~⑩中元素,填写下列空格:
(1)在这10种元素中,非金属性最强的元素是Mg(填“元素符号”),金属性最强的元素是F(填“元素符号”),化学性质最不活泼的元素是Ar(填“元素符号”).
(2)元素①与②中,原子半径较大的是C(填“元素符号”).
(3)元素②与⑦形成的气态氢化物分别是:H2O和H2S(填化学式),两者的热稳定性大小为:前者>后者.(填“>”或“<”).
(4)元素④与⑤的最高价氧化物的水化物的碱性大小为:前者>后者.(填“>”或“<”).
(5)元素⑤的氧化物与盐酸反应的离子方程式为:Al2O3+6H+=2Al3++3H2O.
(6)元素⑤的单质与氢氧化钠溶液反应的化学方程式为:2Al+2NaOH+H2O=2NaAlO2+3H2↑.
(7)元素④和⑧形成的化合物的类型(填离子化合物或共价化合物):离子化合物.
| 周期/族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ⑩ | ② | ③ | ||||
| 三 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
(2)元素①与②中,原子半径较大的是C(填“元素符号”).
(3)元素②与⑦形成的气态氢化物分别是:H2O和H2S(填化学式),两者的热稳定性大小为:前者>后者.(填“>”或“<”).
(4)元素④与⑤的最高价氧化物的水化物的碱性大小为:前者>后者.(填“>”或“<”).
(5)元素⑤的氧化物与盐酸反应的离子方程式为:Al2O3+6H+=2Al3++3H2O.
(6)元素⑤的单质与氢氧化钠溶液反应的化学方程式为:2Al+2NaOH+H2O=2NaAlO2+3H2↑.
(7)元素④和⑧形成的化合物的类型(填离子化合物或共价化合物):离子化合物.
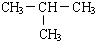 ;
;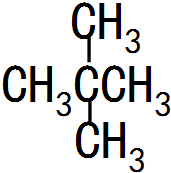 (写结构简式),它的一氯代物有1种.
(写结构简式),它的一氯代物有1种.