题目内容
8.科学探究结果的准确性有赖于探究方法的科学性.某课外活动小组用下图装置探究氯气与氨气之间的反应.其中A、F分别为氨气和氯气的发生装置,C为纯净干燥的氯气与氨反应的装置.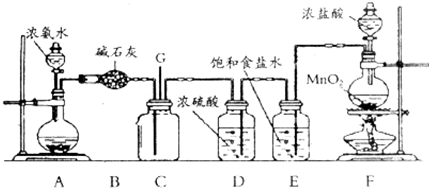
请回答下列问题:
(1)装置F中发生反应的化学方程式为MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O;浓盐酸在该反应中所表现出的性质为还原性、酸性.
(2)装置E的作用是:吸收氯气中的氯化氢.
(3)装置C内出现浓厚的白烟并在容器内壁凝结,另一生成物是空气的主要成分之一.写出反应的化学方程式8NH3+3Cl2═6NH4Cl+N2.
分析 (1)二氧化锰与浓盐酸反应生成氯气、氯化锰和水,依据反应中氯化氢中元素化合价变化判断盐酸表现的性质;
(2)浓盐酸易挥发,该实验中制得的氯气中含有氯化氢杂质,应除去;
(3)由题意可知发生反应为氨气和氯气生成氯化铵和氮气,依据原子个数、得失电子守恒写成反应方程式.
解答 解:(1)装置F中二氧化锰与浓盐酸加热生成氯气,方程式:MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O,反应中有4mol氯化氢参加反应,只有2mol氯离子中的氯化合价升高,所以浓盐酸在反应中既表现还原性,又表现酸性;
故答案为:MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O;
(2)浓盐酸易挥发,该实验中制得的氯气中含有氯化氢杂质,氯化氢易溶于水,氯气在饱和食盐水中溶解度不大,所以可以用E除去;
故答案为:吸收氯气中的氯化氢;
(3)氨气和氯气反应生成白烟氯化铵和空气的主要成分之一氮气,即8NH3+3Cl2═6NH4Cl+N2;
故答案为:8NH3+3Cl2═6NH4Cl+N2.
点评 本题考查了氨气和氯气的制备及性质的检验,熟悉制备原理及二者化学性质是解题关键,题目难度不大.

练习册系列答案
 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案
相关题目
18.太阳能的开发和利用是21世纪一个重要课题.利用储能介质储存太阳能的原理是:白天在太阳照射下某种盐熔化,吸收热量,晚间熔盐固化释放出相应的能量,已知数据:
其中最适宜选用作为储能介质的是( )
| 盐 | 熔点(℃) | 熔化吸热(kJ•mol-1) | 参考价格(元•t-1) |
| CaCl2•6H2O | 29.9 | 37.3 | 780~850 |
| Na2SO4•10H2O | 32.4 | 77.0 | 800~900 |
| Na2HPO4•12H2O | 35.1 | 100.1 | 1 600~2 000 |
| Na2S2O3•5H2O | 45.0 | 49.7 | 1 400~1 800 |
| A. | CaCl2•6H2O | B. | Na2SO4•10H2O | C. | Na2HPO4•12H2O | D. | Na2S2O3•5H2O |
16.下列有关化学用语正确的是( )
| A. | 乙烯的最简式C2H4 | B. | 金刚石的结构模型: | ||
| C. | 溴化钠的电子式: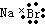 | D. | 臭氧的分子式O3 |
20.下列各组有机物中,仅使用溴水不能鉴别出来的是( )
| A. | 苯 四氯化碳 | B. | 乙炔 乙烯 | C. | 乙烷 乙烯 | D. | 苯 酒精 |
18.长期使用的不锈钢餐具,它也不会生锈的原因是在炼钢的过程中加入了下列物质的( )
| A. | 铬、锰 | B. | 铬、硅 | C. | 铬、镍 | D. | 铬、碳 |
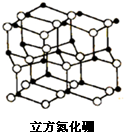 氮化硼是由氮原子和硼原子所构成的晶体,其组成为43.6%的硼和56.4%的氮(质量分数),有多种不同的变体,立方氮化硼是其中一种.立方氮化硼的硬度仅次于金刚石而远远高于其它材料,常用作磨料和刀具材料,其结构与金刚石类似(如图).
氮化硼是由氮原子和硼原子所构成的晶体,其组成为43.6%的硼和56.4%的氮(质量分数),有多种不同的变体,立方氮化硼是其中一种.立方氮化硼的硬度仅次于金刚石而远远高于其它材料,常用作磨料和刀具材料,其结构与金刚石类似(如图).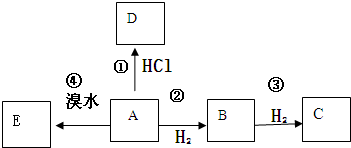
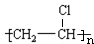 .
.