题目内容
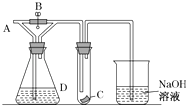
【题目】恒温恒容条件下,下列叙述中不是可逆反应2A(g)+3B(g)![]() 2C(g)达到平衡的标志的是
2C(g)达到平衡的标志的是
①C的生成速率与C的分解速率相等②单位时间生成amolA,同时消耗1.5molB;③各组分的浓度不再变化;④混合气体的密度不再变化;⑤混合气体的总压强不再变化;⑥混合气体的物质的量不再变化;⑦混合气体的平均摩尔质量不再变化;⑧A、B、C的分子数目比为2: 3: 2.
A. ⑤⑥⑧ B. ②⑤⑧ C. ①③④ D. ②④⑦
【答案】A
【解析】试题分析:① C的生成速率与C的分解速率相等,则C的浓度不变,反应达到平衡状态,错误;②单位时间生成amol A,同时会产生1.5amol B,还同时消耗1.5amol B,则反应处于平衡状态,错误;③各组分的浓度不再变化,则物质的总物质的量不变,反应处于平衡状态,错误;④由于是恒温恒容,反应前后物质的质量发生改变,若混合气体的密度不再变化,则任何气体的质量不变,气体的物质的量不变,反应处于平衡状态,错误;⑤该反应是反应前后气体体积不变的反应,在任何时刻混合气体的总压强都再变化,因此不能据此判断反应处于平衡状态,正确;⑥该反应是反应前后气体的物质的量不变的反应,因此在任何时刻混合气体的物质的量都不变,因此不能据此判断反应处于平衡状态,正确;⑦该反应反应前后气体的质量发生变化,而气体的物质的量不变,因此若混合气体的平均摩尔质量不再变化,说明反应处于平衡状态,错误;⑧A、B、C的分子数目比为2:3:2,反应可能处于平衡状态,也可能不处于平衡状态,这与开始加入的物质的量的多少及反应条件有关,错误。因此符合题意的是⑤⑥⑧,选项A正确。

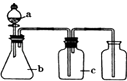
【题目】下表中a、b、c表示相应仪器中加人的试剂,可用如图装置制取、净化、收集的气体是( )
编号 | 气体 | a | b | c |
|
A | NH3 | 浓氨水 | 生石灰 | 碱石灰 | |
B | CO2 | 盐酸 | 碳酸钙 | 饱和NaHCO3溶液 | |
C | NO | 稀硝酸 | 铜屑 | H2O | |
D | Cl2 | 浓盐酸 | 二氧化锰 | 饱和NaCl溶液 |
A.A
B.B
C.C
D.D
【题目】在温度、容积相同的三个密闭容器中发生反应N2(g) + 3H2(g)![]() 2NH3(g) ΔH= -92.4kJ/mol,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下:
2NH3(g) ΔH= -92.4kJ/mol,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下:
容器 | 甲 | 乙 | 丙 |
反应物投入量 | 1molN2、3molH2 | 2molNH3 | 4molNH3 |
NH3的浓度(mol/L) | c1 | c2 | c3 |
反应的能量变化 | 放出a kJ | 吸收b kJ | 吸收c kJ |
体系压强 | P1 | P2 | P3 |
反应物转化率 | α1 | α2 | α3 |
下列说法正确的是
A. 2 c1>c3 B. a + b=92.4 C. 2P1<P3 D. α1 +α3=1