题目内容
【题目】某溶液可能含有Cl-、SO![]() 、CO
、CO![]() 、NH
、NH![]() 、Fe3+、Al3+和K+。取该溶液100mL,加入过量NaOH溶液,加热,得到0.02mol气体,同时观察到红褐色沉淀,过滤,洗涤,灼烧,得到1.6g固体:向上述滤液中加足量BaCl2溶液,得到4.66g不溶于盐酸的沉淀。由此可知原溶液中( )
、Fe3+、Al3+和K+。取该溶液100mL,加入过量NaOH溶液,加热,得到0.02mol气体,同时观察到红褐色沉淀,过滤,洗涤,灼烧,得到1.6g固体:向上述滤液中加足量BaCl2溶液,得到4.66g不溶于盐酸的沉淀。由此可知原溶液中( )
A.CO![]() 、Al3+一定不存在,K+可能存在
、Al3+一定不存在,K+可能存在
B.Cl-一定存在,且c(Cl-)=0.4mol/L
C.SO![]() 、NH
、NH![]() 一定存在,CO32-可能存在
一定存在,CO32-可能存在
D.原溶液中至少存在上述离子中的4种
【答案】D
【解析】
加入过量NaOH溶液,加热,得到0.02mol气体,说明原溶液含有NH![]() ,且n(NH
,且n(NH![]() )=0.02mol,同时观察到红褐色沉淀,说明原溶液含有Fe3+,过滤,洗涤,灼烧,得到1.6g固体为Fe2O3,且可知
)=0.02mol,同时观察到红褐色沉淀,说明原溶液含有Fe3+,过滤,洗涤,灼烧,得到1.6g固体为Fe2O3,且可知![]() ,同时说明不含CO
,同时说明不含CO![]() ,向上述滤液中加足量BaCl2溶液,得到4.66g不溶于盐酸的沉淀为BaSO4,且n=0.02mol,又溶液中必须电荷守恒,即n(NH
,向上述滤液中加足量BaCl2溶液,得到4.66g不溶于盐酸的沉淀为BaSO4,且n=0.02mol,又溶液中必须电荷守恒,即n(NH![]() )+3n(Fe3+)=2n(SO
)+3n(Fe3+)=2n(SO![]() ),带入数据发现,溶液中至少还有0.04mol的Cl-,故c(Cl-)
),带入数据发现,溶液中至少还有0.04mol的Cl-,故c(Cl-)![]() 0.4mol/L。
0.4mol/L。
A.由于Al3+在过量的氢氧化钠中生成沉淀全部溶解,故不一定存在Al3+,故A错误;
B.Cl-一定存在,且c(Cl-)![]() 0.4mol/L,故B错误;
0.4mol/L,故B错误;
C.有溶液中含有Fe3+,故不可能有CO32-存在,故C错误;
D.原溶液中至少存在NH![]() 、Fe3+、SO
、Fe3+、SO![]() 、Cl-,还可能含有K+,故D正确;
、Cl-,还可能含有K+,故D正确;
故答案为:D。

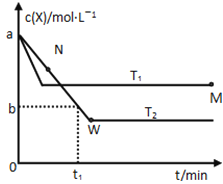
【题目】某温度下,CO(g) + H2O (g)![]() CO2(g)+ H2(g)的平衡常数K=1。该温度下在体积均为1 L的甲、乙两个恒容密闭容器中,投入CO(g) 和 H2O (g)的起始浓度及5min时的浓度如下表所示。
CO2(g)+ H2(g)的平衡常数K=1。该温度下在体积均为1 L的甲、乙两个恒容密闭容器中,投入CO(g) 和 H2O (g)的起始浓度及5min时的浓度如下表所示。
甲 | 乙 | |||
起始浓度 | 5min时浓度 | 起始浓度 | 5min时浓度 | |
c(CO)/mol/L | 0.1 | 0.08 | 0.2 | x |
c(H2O)/mol/L | 0.1 | 0.08 | 0.2 | y |
下列判断不正确的是
A.x = y = 0.16
B.反应开始时,乙中反应速率比甲快
C.甲中0~5min的平均反应速率: v(CO)=0.004"mol/(L·min)
D.平衡时,乙中H2O的转化率是50%,c(CO)是甲中的2倍
【题目】二甲醚是一种重要的清洁燃料,也可替代氟利昂作制冷剂等,对臭氧层无破坏作用。工业上可利用煤的气化产物(水煤气)合成二甲醚。请回答下列问题
(1)煤的气化的主要化学反应方程式为________________
(2)煤的气化过程中产生的有害气体H2S用Na2CO3溶液吸收,生成两种酸式盐,该反应的化学方程式为____________
(3)利用水煤气合成二甲醚的三步反应如下
①2H2(g)+CO(g)=CH3OH(g) △H=-90.8kJ.mo-1
②2CH3OH(g)= CH3OCH3(g)+ H2O(g) △H=-235kJ.mo-1
③CO(g)+H2O(g)=O2(g)+H2(g) △H=-413kJ.mo-1
总反应:3H2(g)+3CO(g)= CH3OCH3(g)+CO2(g)的△H=___________
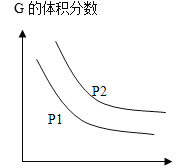
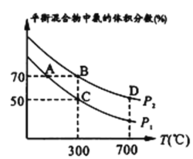
一定条件下的密闭容器中,该总反应达到平衡,要提高CO的转化率,可以采取的措施是____(填字母代号)![]()
a. 高温高压 b.加入催化剂 c.减少CO2的浓度 d.增加Co的浓度 e.分离出二甲醚
(4)已知反应②2CH3OH(g)= CH3OCH3(g)+ H2O(g)某温度下的平衡常数为400.此温度下,在2L密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如下:
物质 | CH3OH | CH3OCH3 | H2O |
物质的量(mol) | 0.88 | 1.2 | 1.2 |
①加入的CH3OH的起始浓度为_________
②比较此时正、逆反应速率的大小:v正________v逆(填少”、“<”或“=”)
③若加入CH3OH后,经10min反应达到平衡,此时CH3OH的转化率a(CH3OH)=_________c(CH3OCH3)=____________