题目内容
【题目】LiPF6是锂离子电池中广泛应用的电解质。某工厂用LiF、PCl5为原料,低温反应制备LiPF6,其流程如下:

已知:HCl的沸点是-85.0 ℃,HF的沸点是19.5 ℃。
(1)第①步反应中无水HF的作用是________________、________________。反应设备不能用玻璃材质的原因是______________________________________________(用化学方程式表示)。无水HF有腐蚀性和毒性,工厂安全手册提示:如果不小心将HF沾到皮肤上,可立即用2%的________溶液冲洗。
(2)该流程需在无水条件下进行,第③步反应中PF5极易水解,其产物为两种酸,写出PF5水解的化学方程式:____________________________________。
(3)第④步分离采用的方法是________;第⑤步分离尾气中HF、HCl采用的方法是________。
(4)LiPF6产品中通常混有少量LiF。取样品w g,测得Li的物质的量为n mol,则该样品中LiPF6的物质的量为________mol(用含w、n的代数式表示)。
【答案】(1)反应物 溶剂 SiO2+4HF=SiF4↑+2H2O NaHCO3
(2)PF5+4H2O=H3PO4+5HF (3)过滤 冷凝(4)
【解析】
试题分析:(1)根据题目中的流程可以看出,固体+液体→新物质+饱和溶液,因此无水HF的作用是反应物和溶剂;反应设备不能用玻璃材质的原因是HF能与二氧化硅反应,腐蚀设备,方程式为:SiO2+4HF=SiF4↑+2H2O;HF属于弱酸,若不小心沾到皮肤上,必须用弱碱性溶液除去,比如2%的NaHCO3溶液;
(2)PF5极易水解,其产物为两种酸,根据元素组成可知,两种酸为:H3PO4和HF,水解的化学方程式为:PF5+4H2O=H3PO4+5HF;
(3)第④步是固液的分离,因此采用过滤的方法;第⑤步分离尾气中HF、HCl,根据HF和HCl的沸点不同,可以采用冷凝法分离;
(4)设LiPF6的物质的量为x,LiF的物质的量为y,则根据Li原子守恒可知,x+y=n;根据质量守恒可知,152x+26y=w,联立两个方程,解得:x=。

【题目】(1).HNO3与金属反应情况多种多样.为探究HNO3性质,某兴趣小组作如下探究:用浓硝酸和水按照不同体积比配成不同浓度的硝酸溶液,各取10mL硝酸溶液分别与铜片反应,实验记录如下:
序号 | 浓硝酸与水的体积比 | 实 验 现 象 |
Ⅰ | 1 ﹕1 | 反应速率快,溶液很快变成蓝色,铜丝表面有大量气泡冒出,气体呈红棕色 |
Ⅱ | 1 ﹕3 | 反应速率较快,溶液变成蓝色,铜丝表面有大量气泡冒出,气体无色 |
Ⅲ | 1 ﹕5 | 反应速率慢,微热后速率加快,溶液变成蓝色,铜丝表面有气泡冒出,气体无色 |
制备NO气体最适宜的是: ,理由是: .
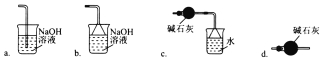
(2).兴趣小组以木炭和浓硝酸为起始原料,探究一氧化氮与过氧化钠反应制备亚硝酸钠。设计装置如下(忽略装置中空气的影响),请回答下列问题:
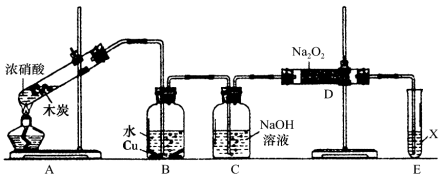
①组装好仪器后,必须进行的一项操作是:_________________。
②推测B中可以观察到的主要现象是:______;C装置的作用是: 。
③装置D中除生成NaNO2外,还有另一种固态物质Y,Y的化学式是:_____。可以通过适当改进,不产生Y物质,请你提出改进方法: _。
④E装置的实验目的是: 。