题目内容
【题目】二甲醚是一种重要的清洁燃料,可替代氟氯代烷作制冷剂,利用水煤气合成二甲醚的三步反应如下:
2H2(g)+CO(g)=CH3OH(g) ΔH=-90.8 kJ·mol-1
2CH3OH(g)=CH3OCH3(g)+H2O(g) ΔH=-23.5 kJ·mol-1
CO(g)+H2O(g)=CO2(g)+H2(g) ΔH=-41.3 kJ·mol-1
请回答下列问题。
(1)由 H2和CO直接制备二甲醚的总反应:3H2(g)+3CO(g)=CH3OCH3(g)+CO2(g)的ΔH=________。一定条件下的密闭容器中,该总反应达到平衡,要提高CO的平衡转化率,可以采取的措施有________(填字母代号)。
a.高温高压 b.加入催化剂 c.分离出CO2
d.增加CO的量 e.分离出二甲醚
(2)某温度下反应2CH3OH(g)![]() CH3OCH3(g)+H2O(g)的平衡常数为400。此温度下,在密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如下:
CH3OCH3(g)+H2O(g)的平衡常数为400。此温度下,在密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如下:
物质 | CH3OH | CH3OCH3 | H2O |
浓度/(mol·L-1) | 0.44 | 0.6 | 0.6 |
①比较此时正、逆反应速率的大小:v正___(填“>”“<”或“=”)v逆。
②若加入CH3OH后,经10 min反应达到平衡,此时c(CH3OH)=________,该时间段内v(CH3OH)=________。
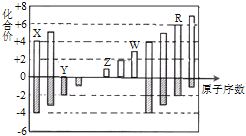
(3)有研究者在催化剂(含Cu—Zn—Al—O和Al2O3)、压强为5.0 MPa的条件下,在相同时间内测得CH3OCH3产率随温度变化的曲线如图甲所示。其中CH3OCH3产率随温度升高而降低的原因可能是_____________________________________。

(4)二甲醚直接燃料电池具有启动快、效率高、能量密度高等优点,可用于电化学降解治理水中硝酸盐的污染。电化学降解NO3-的原理如图乙所示。若电解质为酸性,二甲醚直接燃料电池的负极反应式为____________________;若电解过程中转移了2 mol电子,则阳极室减少的质量为_________g。
【答案】-246.4 kJ·mol-1 c、e > 0.04 mol·L-1 0.04 mol·L-1·min-1 290℃之后,反应达平衡,合成二甲醚的正反应放热,温度升高,平衡向逆向移动产率降低(或温度升高,催化剂失活) CH3OCH3+3H2O-12e-=2CO2↑+12H+ 18
【解析】
(1)已知:①2H2(g)+CO(g)=CH3OH(g) ΔH=-90.8 kJ·mol-1
②2CH3OH(g)=CH3OCH3(g)+H2O(g) ΔH=-23.5 kJ·mol-1
③CO(g)+H2O(g)=CO2(g)+H2(g) ΔH=-41.3 kJ·mol-1
根据盖斯定律,①×2+②+③即得到目标方程式的反应热ΔH4=2ΔH1+ΔH2+ΔH3=-246.4 kJ·mol-1;若提高CO的转化率,则需要减少生成物的浓度、增大H2量、降低温度、增大压强等方法,故c、e正确;
(2)该状态下的浓度商Q=![]() =1.86<400,说明平衡需要向正向移动,此时正反应速率大于逆反应速率;设10min内c(CH3OH)的减少量为2x mol/L,根据化学反应式
=1.86<400,说明平衡需要向正向移动,此时正反应速率大于逆反应速率;设10min内c(CH3OH)的减少量为2x mol/L,根据化学反应式
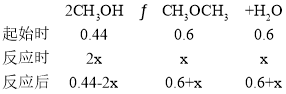
K=![]() ,解得x=0.2,故10min内CH3OH浓度减小0.4mol/L,此时c(CH3OH)=0.04mol/L;这段时间内v(CH3OH)=
,解得x=0.2,故10min内CH3OH浓度减小0.4mol/L,此时c(CH3OH)=0.04mol/L;这段时间内v(CH3OH)=![]() =0.04 mol·L-1·min-1;
=0.04 mol·L-1·min-1;
(3)升高温度二甲醚的产率升高,但是当温度超过290℃的时候,产率下降,原因可能是290℃之后,反应达平衡,合成二甲醚的正反应放热,温度升高,平衡向逆向移动产率降低;
(4)二甲醚直接燃料电池的总反应是:CH3OCH3+3O2=2CO2+3H2O,因电解质溶液是酸性溶液,故负极反应式为CH3OCH3+3H2O-12e-=2CO2↑+12H+;电解过程中Ag-Pt电极的电极方程式为2NO3-+10e-+12H+=N2↑+6H2O,Pt电极的电极方程式为2H2O-4e-=4H++O2↑,电解过程中转移2mol电子,阳极需要消耗18g水。

 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案【题目】将0.2 mol·L-1的KI溶液和0.05 mol·L-1 Fe2(SO4)3溶液等体积混合后,取混合液分别完成下列实验,能说明溶液中存在化学平衡“2Fe3++2I-![]() 2Fe2++I2”的是
2Fe2++I2”的是
实验编号 | 实验操作 | 实验现象 |
① | 滴入KSCN溶液 | 溶液变红色 |
② | 滴入AgNO3溶液 | 有黄色沉淀生成 |
③ | 滴入K3[Fe(CN)6]溶液 | 有蓝色沉淀生成 |
④ | 滴入淀粉溶液 | 溶液变蓝色 |
A. ①和②B. ②和④C. ③和④D. ①和③
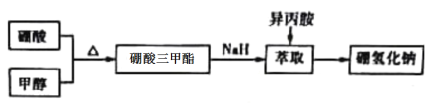
【题目】硼氢化钠(NaBH4)通常为白色粉末,容易吸水潮解,可溶于异丙胺(熔点:-101℃,沸点:33℃)。在有机合成中被称为“万能还原剂”。湿法制备硼氢化钠的流程如下:
请回答有关问题。
Ⅰ.硼酸三甲酯的制备:将硼酸(H3BO3)和适量甲醇加入圆底烧瓶中,然后缓慢地加入浓硫酸,振荡,在烧瓶上加装分馏柱a,用电炉经水浴锅加热,回流2小时,收集硼酸三甲酯与甲醇共沸液。装置如图甲所示(夹持装置略去,下同)。
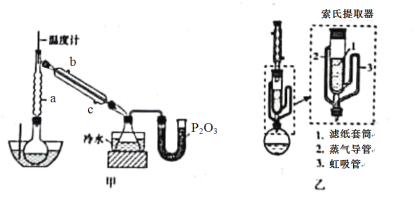
已知,相关物质的性质如下表。
硼酸三甲脂 | 甲醇 | 甲醇钠 | |
溶解性 | 与乙醇、甲醇混溶,能水解 | 与水混溶 | 溶于甲醇,不溶于异丙胺 |
沸点/℃ | 68 | 64 | 450 |
硼酸三甲酯与甲醇混合物的共沸点为54℃ | |||
(1)图甲中分馏柱a的作用是___________;直形冷凝管冷却水应从___________(填“b”或“c”)接口进入。
(2)圆底烧瓶中发生的主要反应的化学方程式为________________________。
(3)本实验采用水浴加热,优点是___________________;U型管中P2O3的作用是_________________。
Ⅱ.“萃取”时,可采用索氏提取法,其装置如图乙所示。实验时烧瓶中溶剂受热蒸发,蒸气沿蒸气导管2上升至球形冷凝管,冷凝后滴入滤纸套筒1中,进行萃取。萃取液液面达到虹吸管3顶端时,经虹吸管3返回烧瓶,从而实现连续萃取。
(4)萃取完全后,硼氢化钠位于______________(填“圆底烧瓶”或“索氏提取器”)中。
(5)与常规的萃取相比,采用索氏提取法的优点是______________。
Ⅲ.某同学欲通过测定硼氢化钠与水反应生成氢气的体积来测定硼氛化钠产品的纯度(杂质与水不反应)。
(6)硼氢化钠与水反应生成氢气和偏硼酸钠,该反应的化学方程式为______________。
(7)该同学称取0.7 g样品,测得生成气体的体积为1.4 L(已折算为标准状况),则样品中硼氢化钠的纯度为________%(结果保留两位有效数字)。