题目内容
5.将C棒、Fe棒平行插人饱和NaCl溶液中(如图所示).下列叙述符合事实的是( )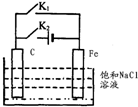
| A. | 断开 K2,闭合 K1时,Fe 电极反应为:2 H++2e-=H2↑ | |
| B. | 断开 K2,闭合 Kl 时,C电极反应为:2Cl--2e-=Cl2↑ | |
| C. | 断开 K1,闭合 K2时,Fe 电极反应为:Fe-2e-=Fe2+ | |
| D. | 断开 Kl,闭合 K2时,C电极反应为:2Cl--2e-=Cl2↑ |
分析 A、断开 K2,闭合 K1时,是原电池装置,活泼的铁是负极,失电子,发生氧化反应;
B、断开 K2,闭合 K1时,是原电池装置,是吸氧腐蚀,C是正极;
C、断开 K1,闭合 K2时,是电解池装置,铁与电源的负极相连是阴极,发生还原反应;
D、断开 K1,闭合 K2时,是电解池装置,C是阳极,还原性强的氯离子首先放电.
解答 解:A、断开 K2,闭合 K1时,是原电池装置,铁是负极发生氧化反应,所以电极反应式:Fe-2e-=Fe2+,故A错误;
B、断开 K2,闭合 K1时,是原电池装置,C电正极发生还原反应,是吸氧腐蚀,所以电极反应式为:O2+4e-+2H2O=4OH-,故B错误;
C、断开 K1,闭合 K2时,是电解池装置,铁是阴极发生还原反应,氢离子得电子,所以电极反应式为:2 H++2e-=H2↑,故C错误;
D、断开 K1,闭合 K2时,是电解池装置,C是阳极,氯离子放电,所以电极反应式为:2Cl--2e-=Cl2↑,故D正确;
故选:D.
点评 本题考查了原电池原理和电解池原理,为高频考点,侧重于学生的分析,能正确判断电池的类型及两极的反应是解本题的关键,题目难度中等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
2. 目前,汽车厂商常利用催化技术将尾气中的NO和CO转化成CO2和N2,化学方程式如下:2NO+2CO$\stackrel{催化剂}{?}$2CO2+N2.为研究如何提高该转化过程反应速率,某课题组进行了以下实验探究.
目前,汽车厂商常利用催化技术将尾气中的NO和CO转化成CO2和N2,化学方程式如下:2NO+2CO$\stackrel{催化剂}{?}$2CO2+N2.为研究如何提高该转化过程反应速率,某课题组进行了以下实验探究.
【资料查阅】
①不同的催化剂对同一反应的催化效率不同;
②使用相同的催化剂,当催化剂质量相等时,催化剂的比表面积对催化效率有影响.
【实验设计】课题组为探究某些外界条件对汽车尾气转化反应速率的影响规律,设计了以下对比实验.
(1)完成以下实验设计表(表中不要留空格).
【图象分析与结论】利用气体传感器测定了三组实验中CO浓度随时间变化的曲线图,如下:
(2)计算第Ⅰ组实验中,达平衡时NO的浓度为3.50×10-3mol/L;
(3)由曲线Ⅰ、Ⅱ可知,增大催化剂比表面积,汽车尾气转化速率增大(填“增大”、“减小”、“无影响”).
 目前,汽车厂商常利用催化技术将尾气中的NO和CO转化成CO2和N2,化学方程式如下:2NO+2CO$\stackrel{催化剂}{?}$2CO2+N2.为研究如何提高该转化过程反应速率,某课题组进行了以下实验探究.
目前,汽车厂商常利用催化技术将尾气中的NO和CO转化成CO2和N2,化学方程式如下:2NO+2CO$\stackrel{催化剂}{?}$2CO2+N2.为研究如何提高该转化过程反应速率,某课题组进行了以下实验探究.【资料查阅】
①不同的催化剂对同一反应的催化效率不同;
②使用相同的催化剂,当催化剂质量相等时,催化剂的比表面积对催化效率有影响.
【实验设计】课题组为探究某些外界条件对汽车尾气转化反应速率的影响规律,设计了以下对比实验.
(1)完成以下实验设计表(表中不要留空格).
| 实验编号 | 实验目的 | T/℃ | NO初始浓度 mol/L | CO初始浓度 mol/L | 同种催化剂的比表面积m2/g |
| Ⅰ | 为以下实验作参照 | 280 | 6.50×10-3 | 4.00×10-3 | 80 |
| Ⅱ | 探究催化剂比表面积对尾气转化速率的影响 | 280 | 6.50×10-3 | 4.00×10-3 | 120 |
| Ⅲ | 探究温度对尾气转化速率的影响 | 360 | 6.50×10-3 | 4.00×10-3 | 80 |
(2)计算第Ⅰ组实验中,达平衡时NO的浓度为3.50×10-3mol/L;
(3)由曲线Ⅰ、Ⅱ可知,增大催化剂比表面积,汽车尾气转化速率增大(填“增大”、“减小”、“无影响”).
10.某原电池装置如图所示.下列有关叙述中,正确的是( )
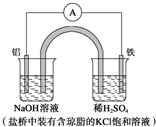

| A. | Fe作正极,发生氧化反应 | |
| B. | 负极反应:Al-3e-+3OH-═Al(OH)3↓ | |
| C. | 工作一段时间后,盛有稀硫酸溶液的杯中pH不变 | |
| D. | 盐桥中的Cl-向左边烧杯中移动,使该烧杯中溶液保持电中性 |
17.下列关于化学反应限度的说法正确的是( )
①一个可逆反应达到的平衡状态就是这个反应在该条件下所能达到的最大限度
②当一个可逆反应达到平衡状态时,正、逆反应速率相等
③平衡状态是一种静止的状态,反应物和生成物的浓度不再改变
④化学反应的限度不可以通过改变条件而改变.
①一个可逆反应达到的平衡状态就是这个反应在该条件下所能达到的最大限度
②当一个可逆反应达到平衡状态时,正、逆反应速率相等
③平衡状态是一种静止的状态,反应物和生成物的浓度不再改变
④化学反应的限度不可以通过改变条件而改变.
| A. | ①② | B. | ③④ | C. | ①③ | D. | ②④ |
14.可以用分液漏斗进行分离的混合物是( )
| A. | 酒精和碘 | B. | 苯和水 | C. | 乙酸和乙酸乙酯 | D. | 乙酸和水 |
 +2nH2O.
+2nH2O.