题目内容
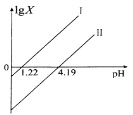
【题目】草酸(H2C2O4)是一种二元弱酸,在菠菜、苋菜、甜菜等植物中含量较高。25℃时,向H2C2O4溶液中滴加NaOH溶液,混合溶液中lgX [X表示 ![]() 或
或![]() 随pH的变化关系如图所示。下列说法不正确的是 ( )
随pH的变化关系如图所示。下列说法不正确的是 ( )
A.直线I中X表示的是![]()
B.直线I、Ⅱ的斜率均为1
C.0.1mol/ L NaHC2O4溶液中:c(Na+)>c(HC2O4-)> c(C2O42-)> c(H2C2O4)
D.已知:25℃时,NH3·H2O的电离常数为10-4.69,则(NH4)2C2O4溶液呈碱性
【答案】D
【解析】
二元弱酸的电离平衡常数Ka1>Ka2,直线Ⅰ表示X与c(H+)乘积等于1×10-1.22,则H2C2O4溶液的Ka1=1×10-1.22,直线Ⅱ表示X与c(H+)乘积等于1×10-4.19,则H2C2O4溶的Ka2=1×10-4.19。
A.直线Ⅰ表示X与c(H+)乘积等于1×10-1.22,平衡常数K=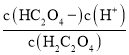 ,与题意不符,A不选;
,与题意不符,A不选;
B.图象中直线Ⅰ表示X与c(H+)乘积等于1×10-1.22,直线Ⅱ表示X与c(H+)乘积等于1×10-4.19,斜率均为1,与题意不符,B不选;
C.HC2O4-的电离平衡常数=1×10-4.19,HC2O4-的水解平衡常数K=![]() =10-12.78,电离程度大于其水解程度,溶液显酸性,则c(Na+)>c(HC2O4-)> c(C2O42-)> c(H2C2O4),与题意不符,C不选;
=10-12.78,电离程度大于其水解程度,溶液显酸性,则c(Na+)>c(HC2O4-)> c(C2O42-)> c(H2C2O4),与题意不符,C不选;
D. 已知:25℃时,NH3·H2O的电离常数为10-4.69,HC2O4-的电离平衡常数=1×10-4.19,HC2O4-电离程度大于NH3·H2O的电离程度,(NH4)2C2O4为相对的强酸弱碱盐,溶液显酸性,符合题意,D可选;
答案为D。

【题目】在80℃时,将0.4mol的四氧化二氮气体充入2L已抽空的固定容积的密闭容器中,隔一段时间对该容器内的物质进行分析,得到如下数据:
时间(s) C(mol/L) | 0 | 20 | 40 | 60 | 80 | 100 |
C(N2O4) | 0. 20 | a | 0.10 | c | d | e |
C(NO2) | 0.00 | 0.12 | b | 0.22 | 0.22 | 0.22 |
反应进行至100s后将反应混合物的温度降低,发现气体的颜色变浅。
(1)该反应的化学方程式为__________________________,表中b_________c(填“<”、“=”、“>”)。
(2)20s时,N2O4的的浓度为__________________mol·L-1,0~20s内N2O4的平均反应速率为________________;
(3)该反应的平衡常数表达式K=___________________
在80℃时该反应的平衡常数K值为:______________(保留到小数点后2位)。
(4)在其他条件相同时,该反应的K值越大,表明建立平衡时____________。
A.N2O4的转化率越高 B.NO2的产量越大
C.N2O4与NO2的浓度之比越大 D.正反应进行的程度越大