题目内容
【题目】以石英、焦炭为原料的部分化工流程如图所示. 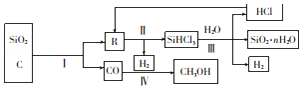
回答下列问题:
(1)反应I在工业上的作用是生产粗硅,为鉴定产品R中是否含有微量的铁单质,取少量R,用稀盐酸溶解,取上层清液后需再加入的试剂是(填字母). a.碘水 b.氯水 c.KSCN溶液 d.NaCl溶液
(2)反应Ⅱ要在干燥环境下迸行,其原因是;经冷凝得到的SiHCl3(沸点为33.0℃)中含有少量SiCl4沸点为57.6℃)和HC1(沸点为﹣84.7℃),则提纯SiHCl3的方法为 .
(3)将水蒸气通过灼热的煤粉可产生水煤气,其主要成分是CO、H2 . 工业上将水煤气液化后制得的CH3OH中含有的化学键类型为(填“离子键”或“共价键”);流程图中的反应Ⅲ为氧化还原反应,其化学方程式为 .
【答案】
(1)bc
(2)防止生成的SiHCl3与水反应;蒸馏
(3)共价键;SiHCl3+(n+2)H2O=SiO2?nH2O+H2↑+3HC1↑
【解析】解:(1)铁能和酸反应生成Fe2+ , Fe2+有还原性,Fe2+能被氯水氧化生成铁Fe3+ , Fe3+遇硫氰化钾溶液变红色,所以可以用氯水和硫氰化钾溶液检验铁的存在;所以答案是:bc;(2)为了防止生成的SiHCl3与水反应,反应Ⅱ要在干燥环境下迸行;沸点不同的液体可以采用蒸馏的方法分离,SiHCl3(沸点为33.0℃)中含有少量SiCl4沸点为57.6℃)和HC1(沸点为﹣84.7℃),这几种物质沸点不同,所以可以采用蒸馏的方法分离;所以答案是:防止生成的SiHCl3与水反应;蒸馏;(3)CH3OH为共价化合物,化学键为共价键;反应III为:SiHCl3+(n+2)H2O=SiO2nH2O+H2↑+3HC1↑; 所以答案是:共价键;SiHCl3+(n+2)H2O=SiO2nH2O+H2↑+3HC1↑.

【题目】不同物质的溶液酸碱性不同,根据下表中pH的情况判断,下列说法中不正确的是( )
盐酸 | CuSO4溶液 | NaCl溶液 | 水 | Na2CO3溶液 | NaOH溶液 | |
pH | <7 | <7 | =7 | =7 | >7 | >7 |
A.酸溶液一定显酸性
B.显碱性的溶液不一定是碱溶液
C.盐溶液一定显中性
D.盐溶液不一定显中性