��Ŀ����
����Ŀ��ij��ѧ��ȤС���ijƷ��������Ħ�����ijɷּ��京����������̽����
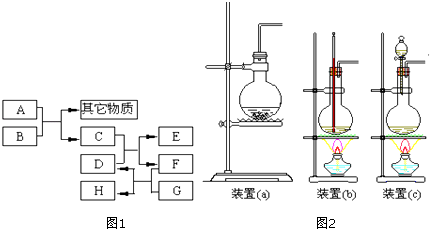
������ϣ�������Ħ������̼��ơ�����������ɣ������������ɷ���������ʱ���������ɡ�������ͼ��ʾװ�ã��г�������ȥ�����Ը�������Ʒ��̼��Ƶĺ������ж����ⶨ��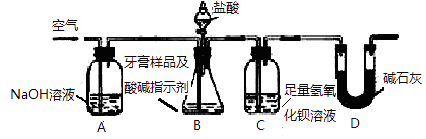
��1��C�з�Ӧ����BaCO3�Ļ�ѧ����ʽ��
��2��װ��D��������
��3��ʵ����������������ͨ������������ó��˿ɽ���B��C�еķ�Ӧ���⣬���У�
��4�����и����ʩ�У�������߲ⶨȷ�ȵ��������ţ���
a.�ڼ�������֮ǰ��Ӧ�ž�װ���ڵ�CO2����
b.�μ�����˹���
c.��A��B֮������ʢ��Ũ�����ϴ��װ��
d.��B��C֮������ʢ�б���̼��������Һ��ϴ��װ��
��5��ʵ����ȷ��ȡ10.00g��Ʒ���ݣ��������βⶨ�����BaCO3ƽ������Ϊ3.94g ������Ʒ��̼��Ƶ���������Ϊ
��6��������Ϊ���زⶨC�����ɵ�BaCO3������ֻҪ�ⶨװ��C������CO2ǰ��������һ������ȷ��̼��Ƶ�����������ʵ��֤�����˷����ⶨ�Ľ������ƫ�ߣ�ԭ������
���𰸡�
��1��CO2��Ba(OH)2��BaCO3����H2O
��2����ֹ��������Cװ�ã����������֣�
��3�������ɵ�CO2����ȫ������C�У�ʹ֮��ȫ������
��4��cd
��5��20%
��6��B�е�ˮ�������Ȼ�������Ƚ���װ��C�У������������𰸣�
��������(1)������̼������������Ӧ����̼�ᱵ��ˮ����Ӧ����ʽΪCO2+Ba(OH)2�TBaCO3��+H2O���ʴ�Ϊ��CO2+Ba(OH)2�TBaCO3��+H2O��
(2)װ��D���Է�ֹ��������Cװ�ã��ʴ�Ϊ����ֹ��������Cװ�ã�
(3)װ���в������ֶ�����̼�����ܱ���ȫ���գ����²ⶨ��̼�ᱵ������ƫС����������ͨ�����������Ϊ�������ɵ�CO2����ȫ������C�У�ʹ֮��ȫ��Ba(OH)2��Һ���գ��ʴ�Ϊ�������ɵ�CO2����ȫ������C�У�ʹ֮��ȫ��Ba(OH)2��Һ���գ�
(4)a���ڼ�������֮ǰ��Ӧ�ž�װ���ڵ�CO2���壬��ֹӰ��̼�ᱵ�����IJⶨ��������߲ⶨȷ�ȣ���a�����ϣ�b���μ�������죬CO2�����������գ����ų�װ��C���μ�����˹��죬ʹ������̼������ȫ��������߲ⶨȷ�ȣ���b�����ϣ�c����AB֮������ʢ��Ũ�����ϴ��װ�ã�����ˮ�֣���Ӱ��CO2 �� ���������߲ⶨȷ�ȣ���c���ϣ�d����BC֮������ʢ�б���̼��������Һ��ϴ��װ��Ba(OH)2 �� ��������CO2�е�HCl��Ӱ��CO2 �� ������߲ⶨȷ�ȣ���d���ϣ���ѡ��cd��
(5)BaCO3����Ϊ3.94g����n(BaCO3)= ![]() =0.02mol����n(CaCO3)=0.02mol������Ϊ0.02mol��100g/mol=2g��������Ʒ��̼��Ƶ���������Ϊ
=0.02mol����n(CaCO3)=0.02mol������Ϊ0.02mol��100g/mol=2g��������Ʒ��̼��Ƶ���������Ϊ ![]() ��100%=20%���ʴ�Ϊ��20%��
��100%=20%���ʴ�Ϊ��20%��
(6)B�е�ˮ�������Ȼ�������Ƚ���װ��C�У����²ⶨ������̼������ƫ�ⶨ��̼��Ƶ�����ƫ��̼��Ƶ���������ƫ�ߣ��ʴ�Ϊ��B�е�ˮ�������Ȼ�������Ƚ���װ��C�С���1��������̼������������Ӧ̼�ᱵ����������
��2�������еĶ�����̼Ҳ��������������Һ��Ӧ��
��3��Ϊ�ⶨ�������뽫ʹ������̼��ȫ��Ӧ��
��4��a���ڼ�������֮ǰ��Ӧ�ž�װ���ڵ�CO2���壬��ֹ�����ж�����̼����C�������������գ�
b���μ�������죬�����ɶ�����̼���죬C�ж�����̼����ȫ�������գ�
c��BC�о�Ϊˮ��Һ������Ҫ���
d���ӷ���HCl����ʢ�б���̼��������Һ��ϴ��װ�û����ɶ�����̼��
��5������̼�ᱵ����������̼��Ƶ�����������
��6��װ���е�ˮ�������Ȼ�������Ƚ���װ��C�У����²ⶨ��̼�ᱵ������ƫ��

����Ŀ������������������NO�ķ�ӦΪ��N2��g��+O2��g��2NO��g����t��ʱ��K=0.09����t���¼ס��ҡ������������ܱ������У�Ͷ��N2��g���� O2��g��ģ�ⷴӦ����ʼŨ�������ʾ�������жϲ���ȷ���ǣ� ��
��ʼŨ�� | �� | �� | �� |
c��N2��/molL��1 | 0.46 | 0.46 | 0.92 |
c��O2��/molL��1 | 0.46 | 0.23 | 0.92 |
A.��ʼʱ����Ӧ���ʣ������ף���
B.ƽ��ʱ��c��NO������=������
C.ƽ��ʱ��N2��ת���ʣ��ף���
D.ƽ��ʱ������c��N2��=0.4 molL��1