题目内容
【题目】已知B为黑色粉末,用D,E,G做焰色反应实验,隔蓝色钴玻璃观察,焰色均呈紫色,F为深红棕色液体,H能使淀粉变蓝,它们之间的相互转化关系如图1所示. 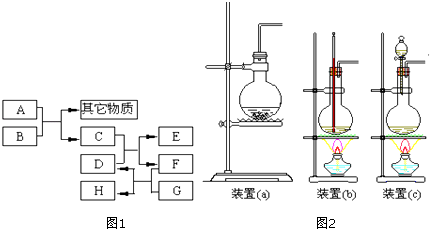
(1)请根据以上关系进行判断,指出下列物质的化学式:
A , C , D , G .
(2)写出下列反应的化学方程式:C+D:;A+B: .
在A和B的反应中,A显示出来的性质是(填写序号,多选倒扣).
①只有还原性;②还原性和酸性;③只有氧化性;④氧化性和酸性
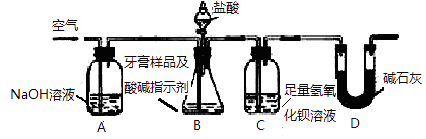
当A和B进行反应时,应选择图2所示装置中的较为合适.
(3)C还能由以下反应制得:KClO3+6HCl=KCl+3Cl2↑+3H2O,在该反应中,被氧化的氯元素与被还原的氯元素的物质的量之比为 .
【答案】
(1)HCl;Cl2;KBr;KI
(2)Cl2+2KRr=2KCl+Br2;MnO2+4HCl(浓) ![]() MnCl2+Cl2↑+2H2O;②;c
MnCl2+Cl2↑+2H2O;②;c
(3)5:1
【解析】解:D、E、G作焰色反应,隔蓝色钴玻璃观察,焰色均呈紫色,则均含K元素,B为黑色粉末,则B为MnO2 , A应为浓盐酸,则C为Cl2 , F为深红棕色液体,H能使淀粉变蓝,F为Br2 , H为I2 , 则D为KBr,E为KCl,G为KI,符合上述转化,(1)由上述分析可知,A为HCl,C为Cl2 , D为KBr,G为KI,所以答案是:HCl;Cl2;KBr;KI;(2)C+D的反应为Cl2+2KRr=2KCl+Br2 , A+B的反应为MnO2+4HCl(浓) ![]() MnCl2+Cl2↑+2H2O,该反应生成氯化锰体现盐酸的酸性,生成氯气体现盐酸的还原性,②符合,该反应为固体和液体反应需要加热,所以用c装置,所以答案是:Cl2+2KRr=2KCl+Br2;MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O,该反应生成氯化锰体现盐酸的酸性,生成氯气体现盐酸的还原性,②符合,该反应为固体和液体反应需要加热,所以用c装置,所以答案是:Cl2+2KRr=2KCl+Br2;MnO2+4HCl(浓) ![]() MnCl2+Cl2↑+2H2O;②;c;(3)KClO3+6HCl=KCl+3Cl2↑+3H2O中,Cl元素的化合价由﹣1价升高为0,失去电子被氧化,5molHCl作还原剂;Cl元素的化合价由+5价降低为0,得到电子被还原,1molKClO3作氧化剂,由电子守恒可知,被氧化的氯元素与被还原的氯元素的物质的量之比为5:1,所以答案是:5:1.
MnCl2+Cl2↑+2H2O;②;c;(3)KClO3+6HCl=KCl+3Cl2↑+3H2O中,Cl元素的化合价由﹣1价升高为0,失去电子被氧化,5molHCl作还原剂;Cl元素的化合价由+5价降低为0,得到电子被还原,1molKClO3作氧化剂,由电子守恒可知,被氧化的氯元素与被还原的氯元素的物质的量之比为5:1,所以答案是:5:1.

【题目】某化学小组在研究Na2SO3溶液、FeCl3溶液性质及反应时,进行了下列实验:
(1)取1molL﹣1的Na2SO3溶液置于空气中,测得其pH随时间的变化曲线如图所示: 
①最初,Na2SO3溶液pH=7.8,解释其原因的离子方程式是 .
②t时间段内,造成其pH发生上述变化,用离子方程式解释是 .
(2)探究Na2SO3溶液与FeCl3溶液实际反应的情况: 实验ⅰ
装置 | 操作 | 现象 |
| 向2mL1molL﹣1FeCl3溶液中,逐滴滴加1moL﹣1Na2SO3溶液2mL | 溶液黄色逐渐加深,最终得红褐色溶液(W) |
实验ⅱ
装置 | 操作 | 现象 |
| 取1mL溶液W于试管中,向其滴加过量盐酸,再滴加5滴BaCl2溶液 | 产生白色沉淀 |
①实验ⅱ证明,溶液中含有离子;
②对Na2SO3溶液与FeCl3溶液实际反应存在两种认识:
认识Ⅰ.反应中Fe3+完全转化为Fe2+ , W溶液中c(Fe2+)一定很大,反应的离子方程式是 .
认识Ⅱ.W溶液中c(Fe2+)应该极小,否则W溶液不会呈红褐色.
(3)资料显示:Fe2+呈淡绿色、FeSO3是墨绿色沉淀、碱式硫酸铁[Fe4(OH)2(SO4)5]溶液为红褐色. ①实验中始终未出现墨绿色沉淀,说明c(Fe2+)极小,其原因用离子方程式解释是 .
②实验过程和结果显示,O2、Fe3+、SO42﹣的氧化性强弱顺序是 .
③若Fe4(OH)2(SO4)5是造成溶液W呈红褐色的原因之一,其形成的化学方程式是 .
④用激光笔照射W溶液,发现有丁达尔现象,用离子方程式解释原因是 .