题目内容
10.在强酸性溶液中能大量共存,并且溶液为无色透明的离子组是( )| A. | K+、Na+、CO32-、NO3- | B. | NH4+、Al3+、SO42-、NO3- | ||
| C. | NH4+、K+、MnO4-、SO42- | D. | Ca2+、Na+、NO3-、HSO3- |
分析 强酸性溶液中存在大量的氢离子,无色透明的溶液中不存在有色离子,
A.碳酸根离子与氢离子反应;
B.四种离子之间不反应,都不与氢离子反应,且为无色溶液;
C.高锰酸根离子为有色离子,不满足溶液无色的条件;
D.酸性条件下,硝酸根离子能够氧化亚硫酸氢根离子.
解答 解:无色溶液可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在,强酸性溶液中存在大量氢离子,
A.CO32-与强酸性溶液中的氢离子反应,在溶液中不能大量共存,故A错误;
B.NH4+、Al3+、SO42-、NO3-之间不发生反应,都不与氢离子反应,且为无色溶液,故B正确;
C.MnO4-为有色离子,不满足溶液无色的要求,故C错误;
D.NO3-、HSO3-在酸性条件下能够发生氧化还原反应,在溶液中不能大量共存,故D错误;
故选B.
点评 本题考查离子共存的正误判断,为中等难度的试题,注意掌握离子反应发生条件,明确离子不能大量共存的一般情况:能发生复分解反应的离子之间,能发生氧化还原反应的离子之间,能发生络合反应的离子之间(如 Fe3+和 SCN-)等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;溶液的颜色,如无色时可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在.

练习册系列答案
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案
相关题目
20.标准状况下,某同学向100mL H2S饱和溶液中通入SO2,所得溶液pH变化如图所示.下列分析中正确的是( )
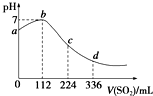

| A. | b点对应的溶液导电性最强 | |
| B. | 亚硫酸是比氢硫酸更弱的酸 | |
| C. | ab段反应是SO2+2H2S═3S↓+2H2O | |
| D. | 原H2S溶液的物质的量浓度为0.05mol•L-1 |
1.化学式为C5H12O2的二元醇有多种同分异构体.其中主链上有3个碳原子和主链上有4个碳原子的二元醇,其同分异构体数目分别是(不包括1个碳原子上连接2个羟基的化合物)( )
| A. | 1和6 | B. | 1和7 | C. | 2和6 | D. | 2和7 |
18.只能用排水集气法的气体是( )
| A. | NH3 | B. | Cl2 | C. | HCl | D. | NO |
5.下列说法不正确的是( )
| A. | 大部分蔬菜和水果属于碱性食物 | B. | 大米和面粉属于酸性食物 | ||
| C. | 牛奶遇碘水变蓝色 | D. | 鸡蛋和牛奶含有较多蛋白质 |
15.下列反应即属于氧化还原反应又属于置换反应的是( )
| A. | Fe2O3+3H2SO4═Fe2(SO4)3+3H2O | B. | 3Cu+8HNO3═3Cu(NO3)2+2NO↑+4H2O | ||
| C. | 2Mg+CO2═C+2MgO | D. | CO+H2O(g)═CO2+H2 |
2.1869年,俄国化学家门捷列夫制作出了第一张元素周期表,揭示了化学元素间的内在联系,成为化学史上的重要里程碑之一.下列有关元素周期表的说法正确的是( )
| A. | 元素周期表含元素最多的族是第ⅢB族 | |
| B. | 元素周期表有18个族 | |
| C. | 第ⅠA族的元素全部是金属元素 | |
| D. | 长周期是指第四、五、六周期 |
1.甲苯苯环上的氢原子被-C4H9取代的同分异构体的种类数有( )
| A. | 3种 | B. | 6种 | C. | 12种 | D. | 18种 |
 .
. .
. 、
、