题目内容
15.下列离子方程式正确的是( )| A. | 把少量SO2通入Ca(ClO)2溶液中:SO2+H2O+Ca2++2ClO-═2HClO+CaSO3↓ | |
| B. | 足量铁屑溶于稀硫酸:2Fe+6H+═2Fe3++3H2↑ | |
| C. | 碳酸氢钙溶液中加入足量烧碱溶液:HCO3-+OH-═CO32-+H2O | |
| D. | 铝片溶于烧碱溶液:2Al+2OH-+2H2O═2AlO2-+3H2↑ |
分析 A.次氯酸根离子能够氧化二氧化硫生成硫酸根离子;
B.不符合反应客观事实,二者反应生成二价铁离子;
C.氢氧化钠过量,反应生成碳酸钙、碳酸钠和水;
D.铝与氢氧化钠溶液反应生成偏铝酸钠和氢气.
解答 解:A.把少量SO2通入Ca(ClO)2溶液中:SO2+H2O+Ca2++3ClO-=CaSO4↓+2HClO+Cl-,故A错误;
B.足量铁屑溶于稀硫酸,离子方程式:Fe+2H+═Fe2++H2↑,故B错误;
C.碳酸氢钙溶液中加入足量烧碱溶液,离子方程式:Ca2++2HCO3-+2OH-═CO32-+2H2O+CaCO3↓,故C错误;
D.铝片溶于烧碱溶液,离子方程式:2Al+2OH-+2H2O═2AlO2-+3H2↑,故D正确;
故选:D.
点评 本题考查了离子方程式的书写,明确离子方程式书写方法及反应实质是解题关键,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
18.“绿色化学”对化学反应提出了“原子经济性”的新概念及要求.理想的原子经济性是原料分子中的原子全部转化为所需要的产物,不产生副产物,实现零排放.下列反应过程一定符合这一要求的是( )
| A. | 甲烷→一氯甲烷 | B. | 氯乙烯→聚氯乙烯 | ||
| C. | 乙醇→乙醛 | D. | 对苯二甲酸,乙二醇→聚酯纤维 |
6.萘(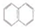 )一氯代物的同分异构体有( )
)一氯代物的同分异构体有( )
 )一氯代物的同分异构体有( )
)一氯代物的同分异构体有( )| A. | 1种 | B. | 2种 | C. | 3种 | D. | 4种 |
10.下列说法正确的是( )
| A. | 用铁片和稀硫酸反应制取氢气时,改用98%的浓硫酸可以加快产生氢气的速率 | |
| B. | 100mL 2mol/L的盐酸跟锌片反应,加入适量的氯化钠溶液,反应速率不变 | |
| C. | SO2的催化氧化是一个放热的反应,所以升高温度,反应的速率减慢 | |
| D. | 在其他条件不变时,使用催化剂只能改变反应速率,而不能改变化学平衡状态 |
20.某有机物甲经氧化后得乙(分子式为C2H302C1),而甲经水解可得丙.1mol丙和2mol乙反应得一种含氯的酯(C6H804Cl2),由此推断甲的结构简式为( )
| A. |  | B. |  | C. | CH2ClCHO | D. | HOCH2CH2OH |
7.已知H2(g)+$\frac{1}{2}$O2(g)═H2O(g);△H=-24l.8kJ/mol下列说法中错误的是( )
| A. | 可推知水的分解反应属于放热反应 | |
| B. | H2与O2(g)反应放出的热量称为中和热 | |
| C. | 1mol H2完全燃烧生成液态水放出的热量小于24l.8kJ | |
| D. | 断开1molH2O的化学键吸收的总能量大于断裂lmolH2和0.5molO2的化学键所吸收的总能量 |
5.能用离子方程式H++OH-→H2O表示的反应是( )
| A. | 稀硫酸和氢氧化钾溶液 | B. | 醋酸和氢氧化钡溶液 | ||
| C. | 氢硫酸和氢氧化钠溶液 | D. | 稀硝酸和氨水 |
