题目内容
【题目】设阿伏加德罗常数的值为NA,下列说法正确的是
A.25°C时,pH=13的氢氧化钡溶液中含有OH-0.1NA个
B.电解精炼铜时,当电路中转移NA个电子,阳极的质量一定减轻了32g
C.0.1 mol H2和0.1 mol I2于密闭容器中充分反应后,其分子总数为0.2NA
D.1 L 0.1 mol·L-1 NH4Cl溶液中,NH4+的数量为0.1NA
【答案】C
【解析】
A.题中没有给出溶液的体积,无法计算出25°C时,pH=13的氢氧化钡溶液中含有OH-的数量,A错误;
B.电解精炼铜时,阳极材料为粗铜,Fe、Zn、Ni、Cu等在阳极失电子,故当电路中转移NA个电子,阳极的质量不一定减轻了32g,B错误;
C.H2+I2 ![]() 2HI,该反应为反应前后气体分子数不变的反应,故0.1 mol H2和0.1 mol I2于密闭容器中充分反应后,其分子总数为0.2NA,C正确;
2HI,该反应为反应前后气体分子数不变的反应,故0.1 mol H2和0.1 mol I2于密闭容器中充分反应后,其分子总数为0.2NA,C正确;
D.NH4Cl为强酸弱碱盐,NH4+在溶液中发生水解反应,故1 L 0.1 mol·L-1 NH4Cl溶液中,NH4+的数量小于0.1NA,D错误;
答案选C。

 名校课堂系列答案
名校课堂系列答案【题目】随着电动自行车市场保有量的不断增加,废弃的铅酸蓄电池已变成不容忽视的一种环境污染源,处理不当会加大对大气、水和土壤的污染。用新方案和新工艺处理废旧铅酸蓄电池,可以达到节能减排、防治污染和资源循环利用的目的。一种处理废旧铅酸蓄电池的流程如下:
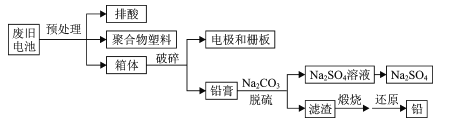
已知:Ksp(PbSO4)=1.6×10-8和Ksp(PbCO3)=7.4×10-14
回答下列问题:
(1)废旧电池预处理时需要将电池放电完全,这样做的目的是____。
(2)写出铅膏脱硫时的离子方程式____。
(3)传统的铅蓄电池的处理工艺是将电池破碎后,洗涤,干燥,直接送入回转炉熔炼。而该工艺使用纯碱脱硫的显著优点是____。
(4)某同学查阅资料发现:儿童从空气中吸入的铅量是成人吸入量的1.6~1.7倍。为了探讨这个现象,展开了相关探究,他通过取样分析,得到了以下实验数据:
离地面高度 | 0.8 | 1.0 | 1.2 | 1.4 | 1.6 | 1.8 | 2.0 |
铅的浓度(μg/cm3) | 1.10 | 0.98 | 0.91 | 0.72 | 0.66 | 0.54 | 0.50 |
①该同学探究的课题名称为____。
②分析以上实验数据,可以得出的结论是___。
③造成此结果的原因可能是____。
(5)在走访调查中,小明同学收集了某铅酸蓄电池处理厂排出的废水样品,为了判断废水中含铅的浓度是否符合排放标准,他设计了如下方案并进行了实验:
![]()
上述实验中如果缺少操作M,所测得结果会 ___(填“偏大”、“偏小”、或“无影响”)。
【题目】二氧化锰不仅是活性好的催化剂,也被广泛用作干电池的正极材料。某化学小组设计用高硫锰矿(主要成分为锰的化合物和硫化亚铁)为原料制取二氧化锰的工艺流程如图:
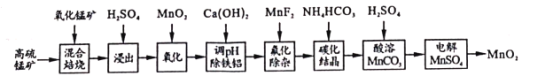
已知:①“混合焙烧”后的烧渣含MnSO4、Fe2O3及少量FeO、MgO、Al2O3
②在该条件下,金属离子开始沉淀和完全沉淀的pH如表:
金属离子 | Fe3+ | Fe2+ | Al3+ | Mn2+ |
开始沉淀 | 1.8 | 6.8 | 4.0 | 7.5 |
完全沉淀 | 3.2 | 8.0 | 5.0 | 8.4 |
(1)写出浸出时与铝元素有关的离子反应方程式____。
(2)上述“氧化”步骤是否可省略____(填“是”或“否”),你的依据是 _____。
(3)“调pH除铁铝’’时,生成沉淀的pH范围为____;“氟化除杂”中除去的离子为____。
(4)请用平衡移动原理解释除杂处理后的Mn2+用NH4HCO3转化成MnCO3沉淀的过程___(用文字和离子方程式表达)。
(5)用惰性电极电解MnSO4制备MnO2时,其阳极反应式为____;整个流程中能够循环利用的物质除MnO2外还有___(写名称)。






