题目内容
下列表示对应化学反应的离子方程式正确的是
| A.用KIO3氧化酸性溶液中的KI: 5I-+IO3-+3H2O =3I2+6OH- |
B.向NH4HCO3溶液中加过量的NaOH溶液并加热: NH4+ +OH- NH3↑+H2O NH3↑+H2O |
| C.将过量SO2通入冷氨水中: SO2+NH3·H2O =HSO3-+NH4+ |
| D.用稀硝酸洗涤试管内壁的银镜: Ag+2H++NO3-=Ag++NO↑+H2O |
C
解析试题分析:A、酸性溶液中不可能出现生成物中含有OH-,正确的离子方程式为: 5I-+IO3-+6H+=3I2+3H2O;错误;B、NaOH过量,HCO3-与OH-会反应生成CO32-和H2O,错误;C项,SO2过量,则生成HSO3-,正确;D项,正确的离子方程式为:3Ag+4H++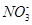 =3Ag++NO↑+2H2O,错误。
=3Ag++NO↑+2H2O,错误。
考点:考查离子方程式的书写。

练习册系列答案
相关题目
下列各组离子能够大量共存的是( )
| A.pH=0的溶液中:Fe3+、Mg2+、Cl—、SO42— |
| B.使pH试纸显蓝色的溶液中:Cu2+、Fe3+、NO3—、SO42— |
| C.滴入甲基橙指示剂呈红色的溶液中:Na+、NH4+、CO32—、NO3— |
| D.水电离出的c(H+)=1×10—13mol·L—1的溶液中:K+、HCO3—、Cl—、NH4+ |
甲、乙、丙是三种不含相同离子的可溶性电解质。它们所含的离子如下表所示:
| 阳离子 | NH4+、Na+、Mg2+ |
| 阴离子 | OH—、NO3—、SO42— |
取等质量的三种化合物配制相同体积的溶液,其物质的量浓度:c(甲)>c(乙)>c(丙),下列说法错误的是
A.甲中一定含Na+ B.乙中一定含NH4+
C.丙中一定含Mg2+ D.丙中一定含SO42—
某Na2CO3、NaAlO2的混合溶液中逐滴加入1mol·L-1的盐酸,测得溶液中的CO32-、HCO3-、AlO2-、Al3+的物质的量与加入盐酸溶液的体积变化关系如图所示。则下列说法不正确的是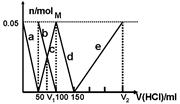
| A.M点时生成的CO2为0mol |
| B.原混合溶液中的CO32-与AlO2-的物质的量之比为1:2 |
| C.V1:V2=1:4 |
| D.a曲线表示的离子方程式为:AlO2-+H+ + H2O=Al(OH)3↓ |
能正确表示下列反应的离子方程式是
| A.向Fe(NO3)2稀溶液中加入盐酸:3Fe2++4H++NO3-===3Fe3++NO↑+2H2O |
B.三氯化铁浓溶液滴入沸水中,制取氢氧化铁胶体Fe3++3H2O Fe(OH)3↓+3H+ Fe(OH)3↓+3H+ |
C.碳酸氢铵溶液与足量的NaOH溶液混合后加热:NH4++OH- NH3↑+H2O NH3↑+H2O |
| D.铝片跟氢氧化钠溶液反应:Al+2OH-=AlO2-+H2↑ |
下列离子方程式不正确的是( )
| A.向100mL0.1mol/L 的溴化亚铁溶液中通入0.05mol的氯气时发生反应的离子方程式:2Fe2++4Br-+3Cl2="2" Fe3++2Br2+6Cl- |
| B.向NH4Al(SO4)2溶液中滴入Ba(OH)2溶液恰好使SO42—完全沉淀:2Ba2++NH4++Al3++2SO42—+4OH-== Al(OH)3↓+NH3·H2O+2BaSO4↓ |
| C.用侯氏制碱法制得NaHCO3 Na++NH3+CO2+H2O=NaHCO3↓+NH4+ |
| D.将Na2O2固体投入H218O中:2H218O+2Na2O2=4OH-+4Na++18O2↑ |
某无色透明的溶液,一定能大量共存的离子组是( )
| A.Cl-、SO42-、Na+、K+ | B.K+、CO32-、Ca2+、NO3- |
| C.HCO3-、Na+、NO3-、H+ | D.NO3-、Cu2+、Cl-、NH4+ |
下列表示对应化学反应的离子方程式正确的是
A.MnO2与浓盐酸反应制Cl2:MnO2+4HCl Mn2++2Cl-+Cl2↑+2H2O Mn2++2Cl-+Cl2↑+2H2O | |
B.醋酸溶解鸡蛋壳:2H++CaCO3=Ca2++CO2↑+ H2O | C.NaHCO3溶液与稀H2SO4反应:CO32-+2H+=H2O+CO2↑ |
| D.向FeCl3溶液中加入Mg(OH)2: 3Mg(OH)2+2Fe3+=2Fe(OH)3+3Mg2+ |