题目内容
某Na2CO3、NaAlO2的混合溶液中逐滴加入1mol·L-1的盐酸,测得溶液中的CO32-、HCO3-、AlO2-、Al3+的物质的量与加入盐酸溶液的体积变化关系如图所示。则下列说法不正确的是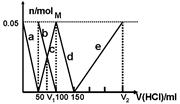
| A.M点时生成的CO2为0mol |
| B.原混合溶液中的CO32-与AlO2-的物质的量之比为1:2 |
| C.V1:V2=1:4 |
| D.a曲线表示的离子方程式为:AlO2-+H+ + H2O=Al(OH)3↓ |
B
解析试题分析:由于酸性顺序是:H2CO3>HCO3->HAlO2,所以向混合溶液中滴加盐酸时,依次的离子反应为(各离子的物质的量[mol]的变化情况):
AlO2-+H++H2O=Al(OH)3↓
0.05 0.05 0.05
CO32-+H+=HCO3-
0.05 0.05 0.05
HCO3-+H+=CO2↑+H2O
0.05 0.05
Al(OH)3+3H+=Al3++3H2O
0.05 0.15
可看出,a曲线表示的是AlO2-的变化情况:AlO2-+H++H2O=Al(OH)3↓
b曲线表示的是CO32-逐渐减少的情况:CO32-+H+=HCO3-,同时,HCO3-增多,由c曲线表示
d曲线表示的是HCO3-的变化情况:HCO3-+H+=CO2↑+H2O
e曲线表示的是Al3+的变化情况:Al(OH)3+3H+=Al3++3H2O
很明显,V1是75ml,而V2是150+150=300ml,V1:V2=l:4
原混合溶液中的CO32-与AlO2-的物质的量均为0.05mol,比值为1:1
M点时根本就没有CO2气体的生成。
考点:考查数形结合的化学计算。

下列各组离子中,在碱性溶液中能共存,且加入硫酸过程中会产生气体和沉淀的是
| A.K+、Na+、AlO2-、CO32- | B.Na+、Cl-、SiO32-、K+ |
| C.Na+、NO3-、AlO2-、K+ | D.Na+、Cl-、HCO3-、Ba2+ |
有一未知的无色溶液,只可能含有以下离子中的若干种(忽略由水电离产生的H+、OH-):H+、NH4+、K+、Mg2+、Cu2+、Al3+、NO3-、CO32-、SO42-,现取三份100mL溶液进行如下实验:
①第一份加足量AgNO3溶液后,有白色沉淀产生。
②第二份加足量BaCl2溶液后,有白色沉淀产生,经洗涤、干燥后,沉淀质量为6.99 g。[
③第三份逐滴滴加NaOH溶液,测得沉淀与NaOH溶液的体积关系如图。根据上述实验,以下推测不正确的是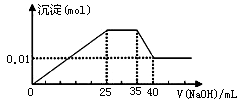
| A.原溶液一定不存在H+、Cu2+、CO32- |
| B.不能确定原溶液是否含有K+、NO3- |
| C.原溶液确定含Mg2+、Al3+、NH4+,且n(Mg2+):n(Al3+):n( NH4+)=1:1:2 |
| D.实验所加的NaOH的浓度为2mol·L-1 |
含有a mol FeBr2的溶液中,通入x mol Cl2。下列各项为通Cl2过程中,溶液内发生反应的离子方程式,其中不正确的是
| A.x=0.3a,2Fe2++Cl2→2Fe3++2Cl- |
| B.x=0.7a,2Br-+Cl2→Br2+2Cl- |
| C.x=1.2a,2Fe2++2Br-+2Cl2→Br2+2Fe3++4Cl- |
| D.x=1.5a,2Fe2++4Br-+3Cl2→2Br2+2Fe3++6Cl- |
下列离子方程式的书写与所给条件相符的是
| A.将4 molCl2通入到含有4 mol FeBr2的溶液中:2Cl2+2Fe2++2Br-= 4Cl-+Br2+2Fe3+ |
| B.已知亚硫酸(H2SO3)的第二级电离常数K2比偏铝酸(HAlO2)的电离常数K要大,则将少量的SO2气体通入到偏铝酸钠溶液中发生的离子反应是:AlO2-+ SO2+2 H2O =Al(OH)3↓+HSO3- |
| C.稀氨水溶液吸收了少量二氧化碳气体: NH3 ·H2O + CO2 = NH4+ + HCO3- |
| D.在明矾溶液中加入氢氧化钡溶液至沉淀质量达到最大时发生的离子反应是: 2Al3+ +3SO42-+3Ba2++6OH-= 3BaSO4↓+2 Al(OH)3↓ |
下列离子方程式书写正确的是
| A.澄清石灰水与少量小苏打溶液混合:Ca2+ +2OH- +2HCO3- = CaCO3↓+ CO32- + 2H2O |
| B.氯化铝溶液中加入过量的氨水:Al3+ + 4NH3·H2O = Al(OH)4-+ 4NH4+ |
| C.漂白粉溶液中通入少量SO2气体:Ca2+ +2ClO- +SO42- +H2O =CaSO3↓+2HClO |
| D.向NH4HSO4稀溶液中逐滴加入Ba(OH)2稀溶液至SO42-刚好沉淀完全: Ba2+ + 2OH- + NH4+ + H+ + SO4 2- = BaSO4↓+ NH3·H2O + H2O |
下列表示对应化学反应的离子方程式正确的是
| A.用KIO3氧化酸性溶液中的KI: 5I-+IO3-+3H2O =3I2+6OH- |
B.向NH4HCO3溶液中加过量的NaOH溶液并加热: NH4+ +OH- NH3↑+H2O NH3↑+H2O |
| C.将过量SO2通入冷氨水中: SO2+NH3·H2O =HSO3-+NH4+ |
| D.用稀硝酸洗涤试管内壁的银镜: Ag+2H++NO3-=Ag++NO↑+H2O |
下列指定溶液中,各组离子可能大量共存的是
| A.pH=1的溶液中:K+、Fe2+、Cl-、NO3- |
| B.在强酸溶液中:Na+、ClO-、Cl-、Ba2+ |
| C.在含有大量Fe3+的溶液中:NH4+、Cl-、Na+、SCN- |
| D.由水电离的c(H+)=10-13mol·L-1的溶液中:Mg2+、Cl-、K+、SO42- |
下列对某些问题的认识正确的是
| A.漂白粉和明矾都常用于自来水的处理,二者的作用原理是相同的 |
| B.SO32-、ClO-、NO3-三种酸根离子在溶液中能大量共存 |
| C.不能用带玻璃塞的玻璃瓶和酸式滴定管盛取碱液,二者的原因是相同的 |
| D.98%的浓硫酸用等体积的水稀释后,硫酸的质量分数为49% |