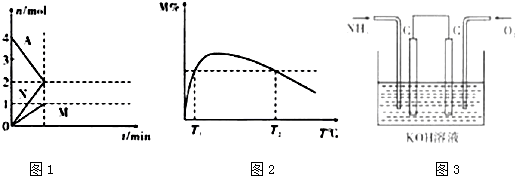
��Ŀ����
7��ij�л���������ת����ϵ��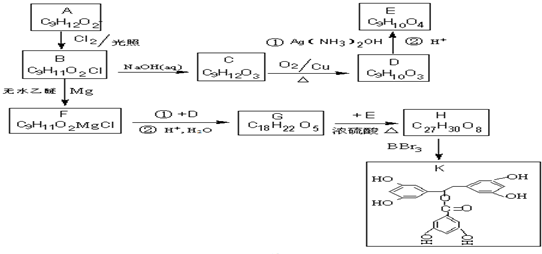
��֪��
��
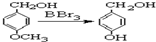
��
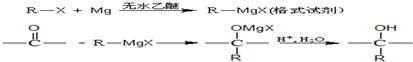
����������Ϣ�ش��������⣺
��1��K�ķ���ʽ��C21H18O8��G��H�ķ�Ӧ������ȡ����Ӧ��
��2��������A����FeCl3��Һ������ɫ��Ӧ���Ʋ���1H�˴Ź����ף�H-NMR������ʾ��4�ֲ�ͬ��ѧ��������ԭ�ӣ��������Ϊ1��2��3��6��
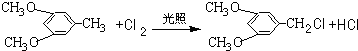
��3��д��A��B��Ӧ�Ļ�ѧ����ʽ��
 ��
����4��д��G�Ľṹ��ʽ��
 ��
����5��������D�ж���ͬ���칹�壬д������������������3��ͬ���칹��
�Ľṹ��ʽ��
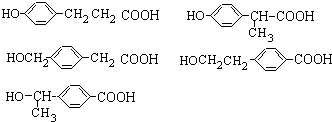 ������3��������
������3�����������ܺ�NaHCO3��Һ��Ӧ����CO2����1mol�л���������Ʒ�Ӧ�ɷų�1molH2��
�۱�����������ȡ�����ұ�����ֻ�����ֲ�ͬ��ѧ��������ԭ�ӣ�
��6����֪������������������Fe/HCl�����±���ԭΪ�������ұ��������ϵİ����ױ����������Լױ�Ϊԭ�ϣ����IJ���Ӧ���ϳ�
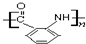 �������Լ���ѡ��������ͼ��ʾ��д����Ӧ����P��Ҫ��Ӧ��������
�������Լ���ѡ��������ͼ��ʾ��д����Ӧ����P��Ҫ��Ӧ��������
���� ��K�Ľṹ��֪A�к��б�����A�IJ����Ͷ�Ϊ$\frac{2��9+2-12}{2}$=4���������������ͼ���A��������������ȡ����Ӧ����B��B����������ˮ��Һ�����µõ�C��������A����FeCl3��Һ������ɫ��Ӧ�����C�ķ���ʽ��֪��A�в������ǻ���C�������������õ�E����C�д���-CH2OH��Aϵ��ת���õ�K�����K�Ľṹ����Ӧ��Ϣ�٣���֪A������2��-OCH3������ȡ�������ڼ�λ����AΪ ��˳�ƿ�֪BΪ
��˳�ƿ�֪BΪ ��CΪ
��CΪ ��DΪ
��DΪ ��EΪ
��EΪ ��FΪ
��FΪ �������Ϣ�ڡ�F��G�ķ���ʽ��K�Ľṹ����֪DΪ
�������Ϣ�ڡ�F��G�ķ���ʽ��K�Ľṹ����֪DΪ ��GΪ
��GΪ ��G��E��Ӧ����H��H��BBr3������-OCH3ת��Ϊ-OH�����H��G�ķ���ʽ��K�Ľṹ����֪EΪ
��G��E��Ӧ����H��H��BBr3������-OCH3ת��Ϊ-OH�����H��G�ķ���ʽ��K�Ľṹ����֪EΪ ��
��
��6���ױ���Ũ������Ũ���������·�����λȡ����Ӧ�����������ױ����ٱ����Ը�������������������������ᣬ��Fe/HCl���������õ��ڰ��������ᣬ��������۷�Ӧ�õ� ��
��
��� �⣺��K�Ľṹ��֪A�к��б�����A�IJ����Ͷ�Ϊ$\frac{2��9+2-12}{2}$=4���������������ͼ���A��������������ȡ����Ӧ����B��B����������ˮ��Һ�����µõ�C��������A����FeCl3��Һ������ɫ��Ӧ�����C�ķ���ʽ��֪��A�в������ǻ���C�������������õ�E����C�д���-CH2OH��Aϵ��ת���õ�K�����K�Ľṹ����Ӧ��Ϣ�٣���֪A������2��-OCH3������ȡ�������ڼ�λ����AΪ ��˳�ƿ�֪BΪ
��˳�ƿ�֪BΪ ��CΪ
��CΪ ��DΪ
��DΪ ��EΪ
��EΪ ��FΪ
��FΪ �������Ϣ�ڡ�F��G�ķ���ʽ��K�Ľṹ����֪DΪ
�������Ϣ�ڡ�F��G�ķ���ʽ��K�Ľṹ����֪DΪ ��GΪ
��GΪ ��G��E��Ӧ����H��H��BBr3������-OCH3ת��Ϊ-OH�����H��G�ķ���ʽ��K�Ľṹ����֪EΪ
��G��E��Ӧ����H��H��BBr3������-OCH3ת��Ϊ-OH�����H��G�ķ���ʽ��K�Ľṹ����֪EΪ ��
��
��1��K�ķ���ʽ��C21H18O8��G��H�ķ�Ӧ�����ǣ�ȡ����Ӧ��
�ʴ�Ϊ��C21H18O8��ȡ����Ӧ��
��2��AΪ ����1H�˴Ź����ף�H-NMR������ʾ��4�ֲ�ͬ��ѧ��������ԭ�ӣ��������Ϊ 1��2��3��6��
����1H�˴Ź����ף�H-NMR������ʾ��4�ֲ�ͬ��ѧ��������ԭ�ӣ��������Ϊ 1��2��3��6��
�ʴ�Ϊ��4��1��2��3��6��
��3��A��B��Ӧ�Ļ�ѧ����ʽ�� ��
��
�ʴ�Ϊ�� ��
��
��4��G�Ľṹ��ʽ�� ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��
��5��������D�� ���ж���ͬ���칹������������������ܺ�NaHCO3��Һ��Ӧ����CO2��˵�������Ȼ�����1mol�л���������Ʒ�Ӧ�ɷų�1molH2��˵���������ǻ����۱�����������ȡ�����ұ�����ֻ�����ֲ�ͬ��ѧ��������ԭ�ӣ�������ͬ��ȡ���������λ������������ͬ���칹���У�
���ж���ͬ���칹������������������ܺ�NaHCO3��Һ��Ӧ����CO2��˵�������Ȼ�����1mol�л���������Ʒ�Ӧ�ɷų�1molH2��˵���������ǻ����۱�����������ȡ�����ұ�����ֻ�����ֲ�ͬ��ѧ��������ԭ�ӣ�������ͬ��ȡ���������λ������������ͬ���칹���У�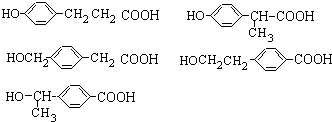 ��
��
�ʴ�Ϊ��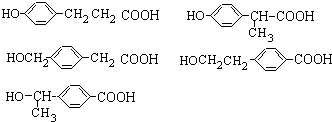 ������3������
������3������
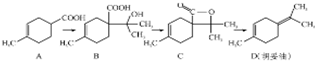
��6���ױ���Ũ������Ũ���������·�����λȡ����Ӧ�����������ױ����ٱ����Ը�������������������������ᣬ��Fe/HCl���������õ��ڰ��������ᣬ��������۷�Ӧ�õ� ���ϳ�·������ͼΪ��
���ϳ�·������ͼΪ�� ��
��
�ʴ�Ϊ�� ��
��
���� ���⿼���л�����ƶ���ϳɣ���������л���ķ���ʽ��K�Ľṹ����Ӧ�������������Ϣ�����ƶϣ��ؼ����ۺϷ���ȷ��A�Ľṹ���ϺõĿ���ѧ�����������������ѶȽϴ�

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�| A�� | 3 | B�� | 4 | C�� | 5 | D�� | 6 |
| A�� | Ϊ�˼ӿ�����ٶȣ����ü�ѹ���˻�߹��˱��ò��������� | |
| B�� | ���������ܶȽϴ�ʱ����Һ���������������������������ŵ��Dz������ٶȿ� | |
| C�� | Ϊ�˼���ͭпԭ����еļ�����������Һ�м���������˫��ˮ | |
| D�� | �������Ǽ���ʳ�κ�ҵ�ε�����Լ�֮һ |
 �����ͣ�D���������ϵ�ԭ�ϣ�������A�ϳɵõ���
�����ͣ�D���������ϵ�ԭ�ϣ�������A�ϳɵõ�������˵����ȷ���ǣ�������
| A�� | ��ϵͳ�������л���A������Ϊ3-��-3-����ϩ���� | |
| B�� | ����������ʣ�B���ܷ����Ӿ۷�Ӧ��Ҳ���ܷ������۷�Ӧ | |
| C�� | C �ķ���ʽΪC10H14O2 | |
| D�� | D ��Br2��CCl4��Һ��Ӧ�������4�������� |
�ز�1��ij�¶Ⱥ�ѹǿ�£�2�������У���ͬʱ������ܱ���ϵ���������ʵ����ʵ���
| ʱ�䣨s�����ʵ�����mol������ | 0 | 10 | 20 | 30 | 40 | 0 | 60 | 70 |
| SO2 | 1 | 0.7 | 0.5 | 0.35 | 0.2 | 0.1 | 0.1 | 0.1 |
| O2 | 0.5 | 0.35 | 0.25 | 0.18 | 0.1 | 0.05 | 0.05 | 0.05 |
| SO3 | 0 | 0.3 | 0.5 | 0.65 | 0.8 | 0.9 | 0.9 | 0.9 |
| ѹǿת�����¶� | 0.1MPa | 0.5MPa | 1MPa | 10MPa |
| 400�� | 99.2 | 99.6 | 99.7 | 99.9 |
| 500�� | 93.5 | 96.9 | 97.8 | 99.3 |
| 600�� | 73.7 | 85.8 | 90.0 | 96.4 |
��1�������ز�1�м���20��30s�ڼ䣬�ö��������ʾ�Ļ�ѧ��Ӧƽ������Ϊ0.0075mol•L-1•s-1��
��2�������ز�2�з����õ�����߸û�ѧ��Ӧ�ȵ�;��������ѹǿ����һ����Χ�ڽ����¶ȣ�
��3�������ز�1���ز�2�з����õ���Ҫʵ���ز�1��SO2��ת��������Ƶķ�Ӧ�������¶�Ϊ600�棬ѹǿΪ1MPa��
| A�� | ��Ƭ��ϡH2SO4��Ӧ | B�� | Ba��OH��2•8H20��NH4CI�ķ�Ӧ | ||
| C�� | ������02�е�ȼ�շ�Ӧ | D�� | ���ȵ�̿��C02��Ӧ |
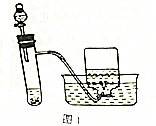
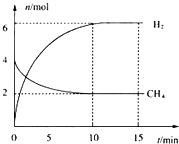 �����Ԫ�صĵ��ʼ��仯���ﱻ�㷺Ӧ���������������У�
�����Ԫ�صĵ��ʼ��仯���ﱻ�㷺Ӧ���������������У�