题目内容
在一定温度下,反应:2A(s)+2B(g)  C(g)+D(g)在恒容容器中进行,不能说明该反应已经达到平衡的是( )
C(g)+D(g)在恒容容器中进行,不能说明该反应已经达到平衡的是( )
 C(g)+D(g)在恒容容器中进行,不能说明该反应已经达到平衡的是( )
C(g)+D(g)在恒容容器中进行,不能说明该反应已经达到平衡的是( )| A.混合气的密度不再随时间而变化 | B.C的质量不再改变 |
| C.容器内的压强不随时间而变化 | D.单位时间内生成2a mol B,同时生成a molD |
C
考查化学平衡状态的判断。密度是混合气的质量和容器容积的比值,容器容积不变,但混合气的质量是变化的,所以A是可以说明的。C是气体,当质量不再变化,即说明其浓度不再变化,因此B可以说明。因为反应前后气体的体积是不变的,所以其压强始终是不变的,C不能说明.选项D中的反应速率方向是相反的,且满足速率之比是相应的化学计量数之比,因此也可以说明。答案选C。

练习册系列答案
相关题目
 C(g) +D(g) 发生过程中的能量变化如图,△H表示反应的焓变。下列说法正确的是( )
C(g) +D(g) 发生过程中的能量变化如图,△H表示反应的焓变。下列说法正确的是( )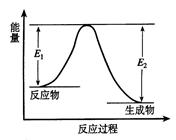
 2SO3(g)。
2SO3(g)。
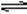 2 NH3达到平衡的标志是( )
2 NH3达到平衡的标志是( )
 109
109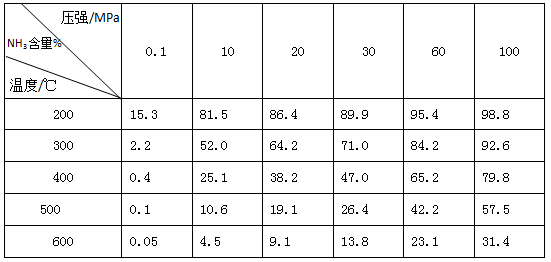
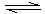 NH3的△H 0(填“>”、“<”或“无法判断”
NH3的△H 0(填“>”、“<”或“无法判断”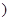 ,请简要说明理由 ;
,请简要说明理由 ; CO2(g)+H2(g),在某一容积为2 L的密闭容器中,加入0.2 mol的CO和0.2 mol的H2O,在催化剂存在的条件下,高温加热,发生如下反应:CO(g)+H2O(g)
CO2(g)+H2(g),在某一容积为2 L的密闭容器中,加入0.2 mol的CO和0.2 mol的H2O,在催化剂存在的条件下,高温加热,发生如下反应:CO(g)+H2O(g)  C(g)+D(g),下列叙述能表明该反应已达到平衡状态的是( )
C(g)+D(g),下列叙述能表明该反应已达到平衡状态的是( )