题目内容
设NA为阿伏加德罗常数的值,下列叙述正确的是
| A.在0.1 mol NaHSO4晶体中阳离子与阴离子总数为0.3 NA |
| B.25℃时,pH=13的1.0 LBa(OH)2溶液中含有的OH-数目为0.2 NA |
| C.常温常压下,4. 4gCO2和N2O混合物中所含有的原子数为0.3 NA |
| D.标准状况下,2. 24LCl2通入足量H2O或NaOH溶液中转移的电子数均为0.1 NA。 |
C
解析试题分析:A .在晶体中存在NaHSO4=Na++HSO4-. n(NaHSO4)=" 0.1" mol ,n(离子)=n(Na+) +n(HSO4-) ="0.1+0.1" = 0.2mol..所以晶体中阳离子与阴离子总数为0.2NA。错误。B.25℃时,pH="13," C(H+)=10-13, C(OH-)="0.1," n(OH-)= 0.1mol/L×1.0L=0.1mol.即0.1 NA。错误。C.CO2和N2O的相对分子质量都是44,所以4. 4gCO2和N2O混合物中所含有的分子数为0.1 NA,由于每个分子中都含有3个原子,所以原子总数为0.3 NA。正确。D.标准状况下,2. 24LCl2的物质的量为0.1mol,但把它通入足量H2O或NaOH溶液中时只有很少一部分发生反应,所以转移的电子数均小于为0.1 NA。错误。
考点:考查阿伏加德罗常数的值在有关物质的量及化学反应计算中的应用的知识。

 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案下列说法正确的是(NA表示阿伏加德罗常数)
| A.1mol钠和足量水反应可生成11.2L氢气 |
| B.常温常压下,32g氧气中含有2NA个氧分子 |
| C.1mol/LK2SO4溶液中,含有2mol钾离子 |
| D.标准状况下,22.4LHCl溶于水后溶液中含有NA个氢离子 |
把200mL NH4HCO3和Na2CO3 的混合溶液分成两等份,取一份加入含amol NaOH的溶液恰好反应完全;取另一份加入含bmol HCl的盐酸恰好反应完全。该混合溶液中c(Na+)为
| A.(l0b - 5a))mol/L | B.(2b-a)mol/L |
C.( )mol/L )mol/L | D.(5b-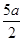 )mol/L )mol/L |
设NA为阿伏加德罗常数的值,下列叙述不正确的( )
| A.10g质量分数为46%的乙醇溶液中,氢原子的总数为0.6NA |
| B.5.6 g铁与足量硫加热充分反应转移电子数为 0.2NA |
| C.50 mL 12 mol?L-1浓盐酸与足量二氧化锰加热反应,转移电子数为0.3 NA |
| D.标准状况下,含有1mol硫原子的SO2 与SO3的混合物,其体积小于22.4L |
10 g 10%的氢氧化钠溶液稀释成50 mL,所得氢氧化钠溶液的物质的量浓度为
| A.0.02 mol/L | B.0.05 mol/L |
| C.0.25 mol/L | D.0.5 mol/L |
设阿伏加德罗常数的值为NA,下列说法中正确的是( )
| A.1mol苯乙烯中含有的C=C数为4NA |
| B.2.8 g乙烯和丙烯的混合气体中所含碳原子数为0.2NA |
| C.0.1molCnH2n+2中含有的C-C键数为0.1nNA |
| D.标准状况下,2.24LCHCl3含有的分子数为0.1NA |
用NA表示阿伏加德罗常数的值,下列说法正确的是
| A.常温常压下,6.4g氧气和臭氧混合气体中含有的原子总数为0.4NA |
| B.常温常压下,22.4LCl2中含有的分子数为NA |
| C.1L1mol·L-1K2SO4溶液中含有的钾离子数为NA |
| D.1mol钠与足量水反应电子转移数为11NA |
下列叙述正确的是( )
| A.常温常压下,17g羟基中所含电子数为9NA |
| B.常温下,1 molFe与足量浓硝酸反应,转移2 NA个电子 |
| C.常温常压下,22.4L的NO2 和CO2混合气体含有2 NA个O 原子 |
| D.在1L0.1 mol/L碳酸钠溶液中,阴离子总数小于0.1 NA |
相同温度和压强下,3体积的X2气体与6体积的Y2气体化合生成6体积的气态化合物A,则生成物A的化学式为 ( )
| A.XY2 | B.X3Y2 | C.X2Y3 | D.XY |