题目内容
标准状况下,均含有NA个电子的H2O和NH3,具有相同的
| A.质量 | B.物质的量 | C.体积 | D.氢原子数 |
B
解析试题分析:水和氨气均是10电子微粒,因此在电子数相同的条件下,水和氨气的物质的量相同。但由于二者的摩尔质量不同,因此质量不同。水含有2个氢原子,氨气含有3个氢原子,则氢原子数不同。标准状况下水不是气体,所以二者的体积也不相同,因此正确的答案选B。
考点:考查物质的量的有关计算

练习册系列答案
相关题目
设NA为阿伏加德罗常数的值。下列说法正确的是
A.0.1 mol羟基(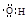 )中含有的电子数为0.7 NA )中含有的电子数为0.7 NA |
| B.1 L 0.1 mol·L-1的AlCl3溶液中含有Al3+的数目为0.1 NA |
| C.0.1 mol N2与足量H2反应,转移的电子数为0.6 NA |
| D.标准状况下,1.12 L HCHO中C原子的数目为0.05 NA |
溶液中只含有Na+、Al3+、Cl-、SO42- 四种离子,已知前三种离子的个数比为3∶2∶1,则溶液中Al3+和 SO42-的离子个数比为 ( )
| A.1∶2 | B.1∶4 | C.3∶4 | D.3∶2 |
下列说法正确的是(NA表示阿伏加德罗常数)
| A.1mol钠和足量水反应可生成11.2L氢气 |
| B.常温常压下,32g氧气中含有2NA个氧分子 |
| C.1mol/LK2SO4溶液中,含有2mol钾离子 |
| D.标准状况下,22.4LHCl溶于水后溶液中含有NA个氢离子 |
将钾与氧形成的化合物或混合物1.02 g溶于水后,可被0.25 mol/L 盐酸 80 mL恰好中和,则该物质的成分可能是
| A.K2O | B.K2O 和K2O2 | C.K2O2 | D.K2O2和KO2 |
下列说法正确的是
| A.等物质的量的甲基(-CH3)与羟基(-OH)所含电子数相等 |
| B.等物质的量浓度的NaOH溶液与氨水中的c(OH-)相等 |
| C.含有相同氧原子数的SO2和CO的质量相等 |
| D.25℃和101kpa,1 mol CO的体积小于22.4L |
下列有关物质结构和性质的叙述正确的是:
①具有16个质子、16个中子和18个电子的微粒符号可表示为:32 16S2-;
②羟基电子式为: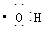 ;
;
③HClO的结构式:H—Cl—O;
④NaHCO3在水中的电离方程式:NaHCO3→Na++H++CO32-;
⑤Na2O的水溶液能导电,这不能说明Na2O是电解质;
⑥SiO2既能与氢氟酸反应又能与NaOH溶液反应,故SiO2是两性氧化物;
⑦分馏、干馏、裂化都是化学变化
| A.①②⑤ | B.①④⑥⑦ | C.②③④⑥ | D.②③⑤⑥⑦ |
把200mL NH4HCO3和Na2CO3 的混合溶液分成两等份,取一份加入含amol NaOH的溶液恰好反应完全;取另一份加入含bmol HCl的盐酸恰好反应完全。该混合溶液中c(Na+)为
| A.(l0b - 5a))mol/L | B.(2b-a)mol/L |
C.( )mol/L )mol/L | D.(5b-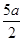 )mol/L )mol/L |
用NA表示阿伏加德罗常数的值,下列说法正确的是
| A.常温常压下,6.4g氧气和臭氧混合气体中含有的原子总数为0.4NA |
| B.常温常压下,22.4LCl2中含有的分子数为NA |
| C.1L1mol·L-1K2SO4溶液中含有的钾离子数为NA |
| D.1mol钠与足量水反应电子转移数为11NA |