题目内容
(9分)(1)下列曲线分别表示元素的某种性质与核电荷数的关系(Z为核电荷数,Y为元素的有关性质)。把与下面元素有关的性质相符的曲线标号填入相应的空格中:
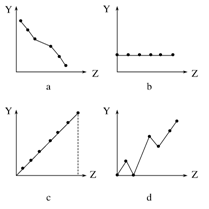
①ⅡA族元素的价电子数 。
②第三周期元素的最高化合价 。
③F-、Na+、Mg2+、Al3+的离子半径 。
(2)元素X、Y、Z、M、N均为短周期主族元素,且原子序数依次增大。已知Y元素原子最外层电子数与核外电子总数之比为3∶4;M元素原子的最外层电子数与电子层数之比为4∶3;N-、Z+、X+的半径逐渐减小;化合物XN常温下为气体。据此回答:
①N的最高价氧化物对应的水化物的化学式为 。
②X、Y、Z元素符号分别为:X 、Y 、Z 。
③工业上制取单质M的化学方程式为_____________________________ 。

①ⅡA族元素的价电子数 。
②第三周期元素的最高化合价 。
③F-、Na+、Mg2+、Al3+的离子半径 。
(2)元素X、Y、Z、M、N均为短周期主族元素,且原子序数依次增大。已知Y元素原子最外层电子数与核外电子总数之比为3∶4;M元素原子的最外层电子数与电子层数之比为4∶3;N-、Z+、X+的半径逐渐减小;化合物XN常温下为气体。据此回答:
①N的最高价氧化物对应的水化物的化学式为 。
②X、Y、Z元素符号分别为:X 、Y 、Z 。
③工业上制取单质M的化学方程式为_____________________________ 。
(1)①b ②c ③a
(2)①HClO4 ②H、O、Na
③SiO2+2C Si+2CO↑
Si+2CO↑
(2)①HClO4 ②H、O、Na
③SiO2+2C
 Si+2CO↑
Si+2CO↑(1)①同主族元素,元素的化合价相同均等于最外层电子数(O、F除外)
②第三周期从左到右,最外层电子数逐渐增多,最高化合价逐渐增大。
③粒子半径大小比较规律:(1)一般来说,电子层数越多,粒子半径越大;(2)电子层数相同,核电荷数越多,半径越小;(3)核电荷数相同,核外电子总数越多,半径越大。
(2)X、Y、Z、M、N对应的元素分别为:H、O、Na、Si、CL
①N的最高价氧化物对应的水化物的化学式为HClO4 ;
②X、Y、Z元素符号分别为:H、O、Na
③工业上制取单质M的化学方程式为SiO2+2C Si+2CO↑
Si+2CO↑
②第三周期从左到右,最外层电子数逐渐增多,最高化合价逐渐增大。
③粒子半径大小比较规律:(1)一般来说,电子层数越多,粒子半径越大;(2)电子层数相同,核电荷数越多,半径越小;(3)核电荷数相同,核外电子总数越多,半径越大。
(2)X、Y、Z、M、N对应的元素分别为:H、O、Na、Si、CL
①N的最高价氧化物对应的水化物的化学式为HClO4 ;
②X、Y、Z元素符号分别为:H、O、Na
③工业上制取单质M的化学方程式为SiO2+2C
 Si+2CO↑
Si+2CO↑
练习册系列答案
相关题目
 间白色沉淀变为灰绿色,最终变为红褐色;
间白色沉淀变为灰绿色,最终变为红褐色; 学原理相
学原理相 s多4个
s多4个
 2NH3
2NH3