题目内容
下列变化中需加入氧化剂才能实现的是( )。
| A.Cl-→Cl2 | B.Fe3+→Fe2+ | C.CuO→Cu | D.H2SO4→BaSO4 |
A
解析试题分析:A选项氯由负一价到零价,化合价升高,被氧化。故需要加入氧化剂。B选项化合价降低,被还原,需加入还原剂。C选项,化合价降低,需加入还原剂。D选项非氧化还原反应。
考点:氧化还原反应。

练习册系列答案
相关题目
Cl2通入70℃的某浓度的氢氧化钠水溶液中,能同时发生两个自身氧化还原反应(未配平):NaOH + Cl2 → NaCl + NaClO + H2O,NaOH + Cl2 → NaCl + NaClO3 + H2O。反应完成后测得溶液中NaClO与NaClO3的数目之比为5:2,则该溶液中NaCl与NaClO的数目之比为
| A.3∶1 | B.2∶1 | C.15∶2 | D.1∶1 |
人体血红蛋白中含有Fe2+离子,如果误食亚硝酸盐,会使人中毒,因为亚硝酸盐会使Fe2+离子转变为Fe3+离子,生成高铁血红蛋白而丧失与O2结合的能力。服用维生素C可缓解亚硝酸盐的中毒,这说明维生素C具有( )
| A.酸性 | B.碱性 | C.还原性 | D.氧化性 |
下列关于氧化还原反应的说法正确是
| A.水在化学反应中既可以作氧化剂,又可以作还原剂 |
| B.1molCl2与足量Fe反应,转移的电子数为3NA |
| C.发生化学反应时失去电子数越多的金属原子,还原能力越强 |
| D.若A2+2D- =2A-+D2,则氧化性:D2>A2 |
有关氧化还原反应的下列说法正确的是
| A.一种元素被氧化,肯定有另一种元素被还原 |
| B.反应中转移电子的数目等于得电子总数与失电子总数之和 |
| C.氧化剂中的元素化合价不一定都降低 |
| D.氧化剂具有氧化性,发生氧化反应 |
反应: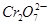 +3
+3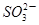 +aH+=2Cr3++3Y+4H2O下列说法不正确的是
+aH+=2Cr3++3Y+4H2O下列说法不正确的是
A.Y是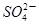 |
| B.a=8 |
C.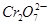 被氧化成 被氧化成 |
D.生成1 mol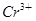 时转移的电子数是3×6.02×1023 时转移的电子数是3×6.02×1023 |
H-是负一价的阴离子,它可与NH3发生以下反应:H-+NH3= H2+NH2-,下列有关这个反应的说法中正确的是
| A.它属于置换反应 |
| B.反应中被氧化和被还原的元素都是H元素 |
| C.该反应中NH3被氧化 |
| D.该反应中H-是氧化剂 |
已知HNO3(浓)和S加热生成NO2,该反应的含硫产物肯定不可能是( )
| A.H2S | B.SO2 | C.SO3 | D.H2SO4 |