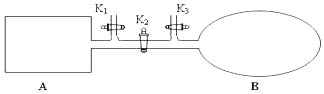
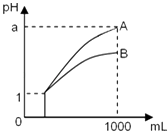
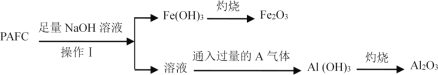题目内容
【题目】碘及其化合物在合成杀菌剂、药物等方面具有广泛用途.回答下列问题:
(1)大量的碘富集在海藻中,用水浸取后浓缩,再向浓缩液中加MnO2和H2SO4 , 即可得到I2 , 写出该反应的离子方程式 .
(2)一种碘和氧的化合物(I4O9),可以称为碘酸碘,则I4O9中碘元素的化合价是 .
A.﹣1
B.+1
C.+3
D.+5
(3)若IOH是两性化合物,写出IOH的酸式电离的电离方程式 .
(4)已知反应2HI(g)═H2(g)+I2(g)△H=+11kJmol﹣1 , 1mol H2(g)、1mol I2(g)分子中化学键断裂时分别需要吸收436kJ、151kJ的能量,则1mol HI(g)分子中化学键断裂时需吸收的能量为kJ.
(5)Bodensteins研究了下列反应:2HI(g)H2(g)+I2(g).在716K时,气体混合物中碘化氢的物质的量分数x(HI)与反应时间t的关系如表:
t/min | 0 | 20 | 40 | 60 | 80 | 120 |
x(HI) | 1 | 0.91 | 0.85 | 0.815 | 0.795 | 0.784 |
x(HI) | 0 | 0.60 | 0.73 | 0.773 | 0.780 | 0.784 |
①根据上述实验结果,该反应的平衡常数K的计算式为: .
②上述反应中,正反应速率为υ正=k正x2(HI),逆反应速率为υ逆=k逆x(H2)x(I2),其中k正、k逆为速率常数,则k逆为(以K和k正表示).
③由上述实验数据计算得到υ正~x(HI)和υ逆~x(H2)的关系可用如图表示.当升高到某一温度时,反应重新达到平衡,相应的点分别为(填字母).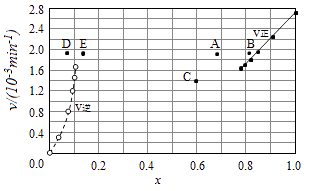
【答案】
(1)2I﹣+MnO2+4H+=Mn2++I2+2H2O
(2)C,D
(3)IOH?H++IO﹣
(4)299
(5)![]() ,
,![]() ,AE
,AE
【解析】解:(1)海藻中的碘元素以碘化物形式存在,反应中I元素发生氧化反应,Mn元素被还原,还原产物应为硫酸锰,反应的离子方程式为:2I﹣+MnO2+4H+=Mn2++I2+2H2O,
所以答案是:2I﹣+MnO2+4H+=Mn2++I2+2H2O;
(2)由题意,碘和氯有相似的化学性质,则碘酸根中碘元素的化合价与氯酸根中氯元素的化合价相同;氯酸钾中钾元素显+1价,氯酸根的化合价为﹣1价,则碘酸根的化合价也为﹣1价;设氯酸根中氯元素的化合价是x,则x+(﹣2)×3=﹣1,x=+5价;因此碘酸根(IO3)中碘元素化合价也为+5价;
碘酸根(IO3)显﹣1价,设I(IO3)3中碘元素的化合价是y,根据在化合物中正负化合价代数和为零,可得:y+(﹣1)×3=0,则y=+3价.
这种化合物中碘的化合价分别是+3和+5价.
所以答案是:CD;
(3)若IOH是两性化合物,IOH的酸式电离生成次碘酸根离子和氢离子,电离方程式为:IOHH++IO﹣,
所以答案是:IOHH++IO﹣;
(4)设1molHI(g)分子中化学键断裂时需吸收的能量为x kJ,则:2x kJ﹣436kJ﹣151kJ=11kJ,解得x=299,
所以答案是:299;
(5)①表中第一列,由HI分解建立平衡,表中第二列向逆反应进行建立平衡,由第一列数据可知,平衡时HI物质的量分数为0.784,则氢气、碘蒸汽总物质的量分数为1﹣0.784=0.216,而氢气、与碘蒸汽物质的量分数相等均为0.108,反应前后气体体积不变,用物质的量分数代替浓度计算平衡常数,则平衡常数K= ![]() =
= ![]() ,
,
所以答案是: ![]() ;
;
②到达平衡时,正、逆反应速率相等,则k正x2(HI)=k逆x(H2)x(I2),则k逆=k正× ![]() =
= ![]() ,
,
所以答案是: ![]() ;
;
③对于2HI(g)H2(g)+I2(g)反应建立平衡时:
升高温度,正、逆反应速率均加快,因此排除C点,正反应为吸热反应,升高温度,平衡向吸热反应方向移动,因此平衡正向移动,再次平衡时HI的物质的量分数减小,因此排除B点,故选A点;
对于H2(g)+I2(g)2HI(g)反应建立平衡时:
升高温度,正、逆反应速率均加快,升高温度,平衡向吸热反应方向移动,因此平衡逆向移动,再次平衡时H2的物质的量分数增大,故选E点;
因此反应重新达到平衡,v正~x(HI)对应的点为A,v逆~x(H2)对应的点为E,
所以答案是:A;E.
【考点精析】根据题目的已知条件,利用化学平衡的计算的相关知识可以得到问题的答案,需要掌握反应物转化率=转化浓度÷起始浓度×100%=转化物质的量÷起始物质的量×100%;产品的产率=实际生成产物的物质的量÷理论上可得到产物的物质的量×100%.

 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案【题目】现使用酸碱中和滴定法测定市售白醋的总酸量(g100mL﹣1).
Ⅰ.实验步骤
(1)用(填仪器名称)量取10.00mL食用白醋,在烧杯中用水稀释后转移到100mL(填仪器名称)中定容,摇匀即得待测白醋溶液.
(2)用酸式滴定管取待测白醋溶液20.00mL于锥形瓶中,向其中滴加2滴作指示剂.
(3)读取盛装0.100 0molL﹣1 NaOH 溶液的碱式滴定管的初始读数.如果液面位置如图所示,则此时的读数为mL.
(4)滴定.当时,停止滴定,并记录NaOH溶液的终读数.重复滴定3次.
(5)Ⅱ.实验记录
滴定次数实验数据(mL) | 1 | 2 | 3 | 4 |
V(样品) | 20.00 | 20.00 | 20.00 | 20.00 |
V(NaOH)(消耗) | 15.95 | 15.00 | 15.05 | 14.95 |
Ⅲ.数据处理与讨论
①按实验所得数据,可得c(市售白醋)=molL﹣1(列式计算);市售白醋总酸量=g100mL﹣1(列式计算).
②在本实验的滴定过程中,下列操作会使实验结果偏大的是填写序号).
a.碱式滴定管在滴定时未用标准NaOH溶液润洗
b.碱式滴定管的尖嘴在滴定前有气泡,滴定后气泡消失
c.锥形瓶中加入待测白醋溶液后,再加少量水
d.锥形瓶在滴定时剧烈摇动,有少量液体溅出.![]()