题目内容
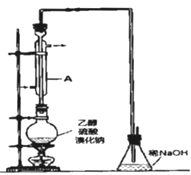
【题目】某化学课外小组用右图装置制取溴苯并探究该反应的类型。先向分液漏斗中加入苯和液溴,再将混合液滴入反应器A(A下端活塞关闭)中。
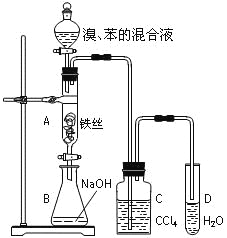
(1)写出A中反应的化学方程式:________________________________________。
(2)实验结束时,打开A下端的活塞,让反应液流入B中,充分振荡,目的是_________________________。
(3)C中盛放CCl4的作用是_____________________________。
(4)若要证明苯和液溴发生的是取代反应,而不是加成反应,通常有两种方法,请按要求填写下表。
向试管D中加入的试剂 | 能证明苯与液溴发生取代反应的现象 | |
方法一 | _____________ | _________________ |
方法二 | _____________ | _________________ |
【答案】![]() +Br2
+Br2![]()
![]() +HBr 除去溶于溴苯中的溴 除去溴化氢气体中的溴蒸气 AgNO3溶液 产生淡黄色沉淀 石蕊试液 溶液变红色
+HBr 除去溶于溴苯中的溴 除去溴化氢气体中的溴蒸气 AgNO3溶液 产生淡黄色沉淀 石蕊试液 溶液变红色
【解析】
(1)苯与溴在催化剂存在下发生取代反应生成溴苯和溴化氢,A中反应的化学方程式为![]() +Br2
+Br2![]()
![]() +HBr;
+HBr;
(2)A中制得的溴苯中混有未反应的溴,B中盛有NaOH溶液,实验结束时,打开A下端的活塞,让反应液流入B中,充分振荡,目的是除去溶于溴苯中的溴,反应的方程式为Br2+2NaOH=NaBr+NaBrO+H2O;
(3)由于反应放热,苯和液溴均易挥发,所得HBr中混有苯蒸气和溴蒸气,C中盛放CCl4的作用是除去HBr气体中的溴蒸气,以防干扰HBr的检验;
(4)如果发生取代反应,则有HBr生成,HBr易溶于水电离出H+和Br-,只要检验试管D中含H+或Br-即可证明苯和液溴发生的是取代反应;方法一:检验Br-,向试管D中滴加硝酸银溶液,如果生成淡黄色沉淀就证明含有溴离子,进而证明发生了取代反应;方法二:检验H+,向试管D中滴加石蕊试液,若溶液变红色就证明含有氢离子,进而证明发生了取代反应。

 教学练新同步练习系列答案
教学练新同步练习系列答案 课前课后同步练习系列答案
课前课后同步练习系列答案 课堂小作业系列答案
课堂小作业系列答案【题目】在100 ℃时,将0.40 mol二氧化氮气体充入一个2 L抽空的密闭容器中,发生反应:2NO2![]() N2O4。每隔一段时间就对该容器内的物质进行分析,得到下表数据:
N2O4。每隔一段时间就对该容器内的物质进行分析,得到下表数据:
时间/s | 0 | 20 | 40 | 60 | 80 |
n(NO2)/mol | 0.40 | n1 | 0.26 | n3 | n4 |
n(N2O4)/mol | 0.00 | 0.05 | n2 | 0.08 | 0.08 |
(1)在上述条件下,从反应开始至20 s时,用二氧化氮表示的平均反应速率为_______mol/(L·s)。
(2)该反应的平衡常数K的数值为____。
(3)若在相同条件下最初向该容器中充入四氧化二氮气体,要达到上述平衡状态,四氧化二氮的起始浓度是______mol·L-1。
(4)达到平衡后,如果升高温度,气体颜色会变深,则升高温度后,反应2NO2![]() N2O4的平衡常数将_________(填“增大”“减小”或“不变”)。
N2O4的平衡常数将_________(填“增大”“减小”或“不变”)。
(5)达到平衡后,如果向该密闭容器中再充入0.32 mol He,并把容器体积扩大为4 L,则平衡将_______(填“向左移动”“向右移动”或“不移动”)。