题目内容
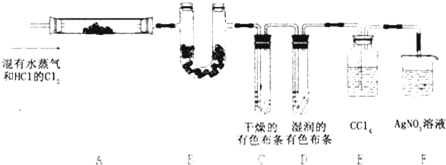
某校化学实验兴趣小组为了探究在实验室制备Cl2的过程中有水蒸气和HCl挥发出来,同时证明氯气的某些性质,甲同学设计了如图所示的实验装置(支撑用的铁架台省略),按要求回答问题.(已知氯化氢不溶于CCl4)
(1)写出上图中制备氯气的化学方程式
(2)①装置B中盛放的试剂为
②装置C中盛放的试剂为
③根据装置D和E中出现的不同现象,得出的结论是
(3)乙同学认为甲同学的实验有缺陷,不能确认最终通入AgNO3溶液中的气体只有一种.为了保证实验结论的可靠性,乙同学提出在某两个装置之间再加一个装置.你认为该装置中应放入
(4)次氯酸钠固体与浓盐酸混合也能反应制备氯气,写出反应方程式
分析:(1)实验室用二氧化锰与浓盐酸反应制备氯气;
(2)①利于无水硫酸铜遇到水变蓝性质检验氯气中是否含有水蒸气;
②用C装置吸收氯气中的水蒸气,氯气与碱反应应选用酸性干燥剂;
③依据干燥的有色布条不褪色,湿润的有色布条褪色,对比说明具有漂白性的不是氯气;
(3)氯气能氧化碘化钾得到单质碘,碘与淀粉变蓝;
(4)次氯酸钠固体具有强的氧化性氧化浓盐酸中的氯化氢生成氯气、氯化钠和水.
(2)①利于无水硫酸铜遇到水变蓝性质检验氯气中是否含有水蒸气;
②用C装置吸收氯气中的水蒸气,氯气与碱反应应选用酸性干燥剂;
③依据干燥的有色布条不褪色,湿润的有色布条褪色,对比说明具有漂白性的不是氯气;
(3)氯气能氧化碘化钾得到单质碘,碘与淀粉变蓝;
(4)次氯酸钠固体具有强的氧化性氧化浓盐酸中的氯化氢生成氯气、氯化钠和水.
解答:解:(1)A.二氧化锰与浓盐酸反应生成氯化锰、水、氯气,方程式为:MnO2+4HCl
MnCl2+Cl2↑+2H2O,
故答案为:MnO2+4HCl
MnCl2+Cl2↑+2H2O;
(2)①为了探究在实验室制备Cl2的过程中有水蒸气,可以在B中加入无水硫酸铜,如果固体变蓝则证明氯气中含有水蒸气,
故答案为:无水硫酸铜;
②为了除去氯气中的水蒸气,选用浓硫酸做干燥剂,所以C中盛放的是:浓硫酸,
故答案为:浓硫酸;
③干燥的有色布条不褪色,湿润的有色布条褪色,说明具有漂白性的不是氯气,而是次氯酸,
故答案为:氯气无漂白性,次氯酸有漂白性;
(3)氯气与碘化钾发生反应:Cl2+2KI=2KCl+I2,碘遇淀粉变蓝,所以可以在F和G之间连接一个盛有湿润的淀粉碘化钾试纸的洗气瓶检验是否存在氯气,
故答案为:湿润的淀粉KI试纸;
(4)次氯酸钠固体与浓盐酸反应的化学方程式为:NaClO+2HCl=NaCl+Cl2↑+H2O,
故答案为:NaClO+2HCl=NaCl+Cl2↑+H2O.
| ||
故答案为:MnO2+4HCl
| ||
(2)①为了探究在实验室制备Cl2的过程中有水蒸气,可以在B中加入无水硫酸铜,如果固体变蓝则证明氯气中含有水蒸气,
故答案为:无水硫酸铜;
②为了除去氯气中的水蒸气,选用浓硫酸做干燥剂,所以C中盛放的是:浓硫酸,
故答案为:浓硫酸;
③干燥的有色布条不褪色,湿润的有色布条褪色,说明具有漂白性的不是氯气,而是次氯酸,
故答案为:氯气无漂白性,次氯酸有漂白性;
(3)氯气与碘化钾发生反应:Cl2+2KI=2KCl+I2,碘遇淀粉变蓝,所以可以在F和G之间连接一个盛有湿润的淀粉碘化钾试纸的洗气瓶检验是否存在氯气,
故答案为:湿润的淀粉KI试纸;
(4)次氯酸钠固体与浓盐酸反应的化学方程式为:NaClO+2HCl=NaCl+Cl2↑+H2O,
故答案为:NaClO+2HCl=NaCl+Cl2↑+H2O.
点评:本题考查了氯气的制备和性质的检验,题目综合性较强,难度中等,本题注意(3)实验装置和试剂的选择.

练习册系列答案
 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案
相关题目
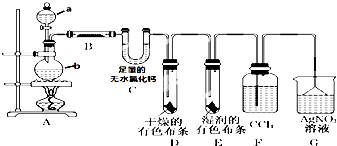 某校化学实验兴趣小组为了探究在实验室制备Cl2的过程中有水蒸气和HCl挥发出来,同时证明氯气的某些性质,甲同学设计了如图所示的实验装置(支撑用的铁架台省略),按要求回答问题.(1)①分别写出a、b的实验仪器名称
某校化学实验兴趣小组为了探究在实验室制备Cl2的过程中有水蒸气和HCl挥发出来,同时证明氯气的某些性质,甲同学设计了如图所示的实验装置(支撑用的铁架台省略),按要求回答问题.(1)①分别写出a、b的实验仪器名称