题目内容
【题目】洋蓟素是一种新结构类型的抗乙型肝炎病毒和抗艾滋病病毒的化合物,其结构如图所示,有关洋蓟素的说法正确的是( )
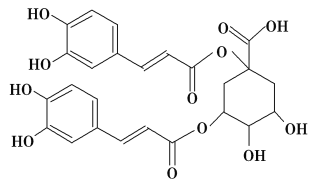
A. 1 mol洋蓟素最多可与6 mol Br2反应
B. 1 mol洋蓟素含6 mol酚羟基
C. 一定条件下能发生酯化反应和消去反应
D. 1 mol洋蓟素最多可与9 mol NaOH反应
【答案】C
【解析】
A.洋蓟素苯环上酚羟基的邻、对位氢原子可以被Br2取代,![]() 可以与Br2发生加成反应,故1 mol 洋蓟素最多可与8 mol Br2反应,故A错误;B.1 mol洋蓟素含有4 mol酚羟基,故B错误;C.羟基、羧基可以发生酯化反应,醇羟基所连碳原子的邻位碳原子上有氢原子,则可以发生消去反应,故C正确;酚羟基、酯基、羧基均可以消耗NaOH,故1 mol洋蓟素可以最多消耗7 mol NaOH,故D错误;答案选C。
可以与Br2发生加成反应,故1 mol 洋蓟素最多可与8 mol Br2反应,故A错误;B.1 mol洋蓟素含有4 mol酚羟基,故B错误;C.羟基、羧基可以发生酯化反应,醇羟基所连碳原子的邻位碳原子上有氢原子,则可以发生消去反应,故C正确;酚羟基、酯基、羧基均可以消耗NaOH,故1 mol洋蓟素可以最多消耗7 mol NaOH,故D错误;答案选C。

【题目】用如图所示装置进行下列实验,实验结果与预测的现象不一致的是( )
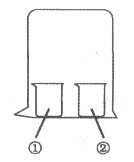
①中的物质 | ②中的物质 | 预测①的现象 | |
A | 淀粉KI溶液 | 浓硝酸 | 无明显变化 |
B | 酚酞溶液 | 浓盐酸 | 无明显变化 |
C | MgCl2溶液 | 浓氨水 | 有白色沉淀 |
D | 湿润红纸条 | 饱和氯水 | 红纸条褪色 |
A. AB. BC. CD. D
【题目】下列实验操作和实验结论均正确的是
实验操作 | 实验结论 | |
A | 先加少量氯水,再滴加KSCN溶液,出现血红色 | 证明某溶液中存在Fe2+ |
B | 向AgCl悬浊液中加入NaI溶液时出现黄色沉淀 | Ksp(AgCl)<Ksp(AgI) |
C | 向碳酸钙中滴加盐酸,有气泡产生 | 证明氯的非金属性大于碳 |
D | 将MgCl2溶液在氯化氢的气流中蒸发、结晶、过滤 | 制备氯化镁晶体 |
A. A B. B C. C D. D
【题目】前四周期元素 R、X、Y、Z、E的原子序数依次增加,它们的结构和部分信息如下表所示:
元素代号 | 部分信息 |
R | 基态R原子核外有三个能级,每个能级上电子数相同 |
X | X的双原子单质δ键和π键数目之比为1∶2 |
Y | 短周期主族元素中,原子半径最大 |
Z | Z的最高正化合价与最低负化合价之和等于4 |
E | 基态E3+的外围电子排布式是3d5 |
回答问题:
(1)E元素在周期表中的位置是________,其基态原子中电子占据的最高能层是__________________。
(2)元素 X的氢化物M,分子内含18个电子,M的结构式为_____,每个中心原子的价层电子对数是_________________。
(3)在R、X、Z的含氧酸根离子中,互为等电子体的离子组是_________________。
(4)Z元素的两种氧化物对应的水化物中,酸性较强的________,其原因是_________________。
(5)(ZX)4在常压下,高于130℃时(ZX)4分解为相应的单质,这一变化破坏的作用力是________________;它为热色性固体,具有色温效应,低于-30℃时为淡黄色,高于100℃时为深红色.
在淡黄色→橙黄色→深红色的转化中,破坏的作用力是_________________。
(6)常温条件下,E的晶体采用如图所示的堆积方式。则这种堆积模型的配位数为__________,若E原子的半径为r,则单质E的原子空间利用率为________________。(列出计算式即可)