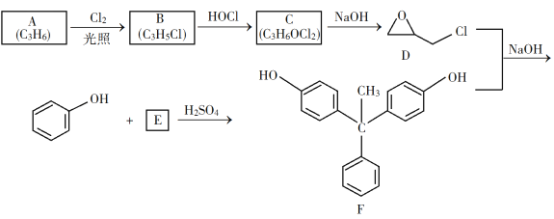
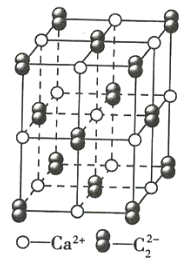
��Ŀ����
����Ŀ����п����(����ZnS��SiO2������FeS����)���Ѱ�Һ(��H2SO4Լ20%����������Fe2+��TiO2+)�������Ѱ�Һ����п��������������ˮ������п���̼����£�

�ش��������⣺
(1)�ڱ��չ����У������˾���Ư���Ե�����ͽ������������������_________������X����Ҫ�ɷ���_________________��
(2)����ʱ���������������㣬�����__________������H2TiO3��������ӷ�Ӧ����ʽΪ____________��������ʵ�ʿ��ǣ���pHʱ��ѡ�����ʯ����������ռ��ԭ����_________��
(3)�����£���ҺY��п����Ũ��ԼΪ6mol/L����Ksp[Fe(OH)3]=4.0��10-38��Ksp[Zn(OH)2]=6.0��10-18���ݴ˷���������ʯ������ڵ�pHӦ������________����ʱ��Һ�л��е�����������ΪH+��__________��
(4)��ҵ�ϣ����õ�������İ���п(II)��Һ����[Zn(NH3)4]2+���Ʊ�����п���������ĵ缫��ӦʽΪ__________��
���𰸡�SO2����������� SiO2����������裩 Fe2����������ȫ���ڵ���pHʱ���ܳ���Fe2�� 2H2O��TiO2��=H2TiO3����2H����TiO2����Ca(OH)2=H2TiO3��Ca2�� Ca(OH)2��Դ�㣬�۸���� 5 Ca2�� [Zn(NH3)4]2����2e��=Zn��4NH3
��������
��п�����չ�����ZnS��FeS����O2��Ӧ�����ɽ����������SO2�������Ѱ�Һ����������������Ѱ�Һ�е�H2SO4��Ӧ����������ˮ�������Ρ����ˣ����������SiO2����ȥ��ͨ����������Fe2����Fe3+������ʯ�������pH���Ա�ת��ΪFe(OH)3������ȥ��TiO2��Ҳת��ΪH2TiO3������ȥ�����˵õ�ZnSO4��Һ�����õ�ZnSO4��7H2O��
(1)����Ϣ��֪�����չ��з�����Ӧ��2ZnS��3O2 ![]() 2ZnO��2SO2��4FeS��7O2
2ZnO��2SO2��4FeS��7O2![]() 2Fe2O3��4SO2�����Էų���������SO2������ZnO��Fe2O3���������ᣬSiO2������H2SO4���������XΪSiO2��
2Fe2O3��4SO2�����Էų���������SO2������ZnO��Fe2O3���������ᣬSiO2������H2SO4���������XΪSiO2��
(2)ͨ�������Ŀ����Ϊ�˽�Fe2������ΪFe3���Ӷ��γ�Fe(OH)3��ȥ������������㣬Fe2��û�б���ȫ�������ڵ���pHʱ��������ȫ��ȥFe2����
����ʯ�������pH��TiO2��ת��ΪH2TiO3���������ϼۿ�֪��Ti�Ļ��ϼ�û�з����仯������ԭ���غ���ƽ����ѧ����ʽΪ2H2O��TiO2��=H2TiO3����2H����TiO2����Ca(OH)2=H2TiO3��Ca2����
����ʵ�ʿ���ʱ�����뿼��ԭ�ϵ���Դ�ͼ۸�ʯ����Ca(OH)2��Դ�㣬�۸���ˣ�
(3)����pHʱ��Fe3��Ҫ������ȫ����Zn2�����ܳ���������Fe3��������ȫ��Ũ��Ϊ1��10��5mol��L��1��c(Fe3��)3c(OH��)= Ksp[Fe(OH)3]=4.0��10-38�������c(OH��)=1.6��10��11mol��L��1����Zn2��ǡ�ó���ʱ��c(Zn2��)2c(OH��)= Ksp[Zn(OH)2]=6.0��10-18��c(Zn2��)=6mol/L�������c(OH��)=10��9mol��L��1����c(OH��)��Ӧ����10��9mol��L��1���ɼ�������pHֵ��![]() �����pHӦ������5��
�����pHӦ������5��
����ʯ����Ca(OH)2����pHʱ�����ɵ�CaSO4����������Һ�л�����Ca2����
(4)������Ϣ����[Zn(NH3)4]2���Ʊ�Zn�����������õ��ӷ�����ԭ��Ӧ����缫��ӦΪ[Zn(NH3)4]2����2e��=Zn��4NH3��

����Ŀ����2molSO2��1molO2�����������ɱ䣬ѹǿ�㶨���ܱ������У���һ���¶��·������·�Ӧ��2SO2(g)+O2(g)![]() 2SO3(g) ��H��0������Ӧ���е�ʱ��t1��ʱ�ﵽƽ��״̬����û�����������ʵ���Ϊ2.1mol���Իش��������⣺
2SO3(g) ��H��0������Ӧ���е�ʱ��t1��ʱ�ﵽƽ��״̬����û�����������ʵ���Ϊ2.1mol���Իش��������⣺
��1����ƽ��ʱ���������ΪaL��д���÷�Ӧ��ƽ�ⳣ��Ϊ��K=__________���ú�a�Ĵ���ʽ��ʾ��
��2����Ӧ���е�t1ʱ��SO2���������Ϊ_______________��
��3������t1ʱ����һ�����������Ar����SO2�����ʵ�����________�����������С�����䡱����
��4������t1ʱ���£����´ﵽƽ��״̬����ƽ������������������ʵ���____2.1mol�����������������=��������˵��ԭ��____________��
��5����t1�ﵽƽ�����������������ٱ仯���ټ���0.2molSO2��0.1molO2��1.8molSO3����ʱv��________v�� �����������������=������
��6��һ���¶��£��������ݻ���ͬ�ĺ����ܱ������а���ͬ��ʽͶ�뷴Ӧ�������Ӧ2SO2(g)+O2(g)![]() 2SO3(g)������Ӧ���ȣ�����÷�Ӧ������������£�
2SO3(g)������Ӧ���ȣ�����÷�Ӧ������������£�
����1 | ����2 | ����3 | |
��Ӧ�¶�T/K | 700 | 700 | 800 |
��Ӧ��Ͷ���� | 2 mol SO2��1 mol O2 | 4 mol SO3 | 2 mol SO2��1 mol O2 |
ƽ��v��(SO2)/ mol��L��1��s��1 | v1 | v2 | v3 |
ƽ��c(SO3)/mol��L��1 | c1 | c2 | c3 |
ƽ����ϵ��ѹǿp/Pa | p1 | p2 | p3 |
���ʵ�ƽ��ת������ | ��1(SO2) | ��2(SO3) | ��3(SO2) |
ƽ�ⳣ��K | K1 | K2 | K3 |
�á���������������=���������к����ϣ�
c2______2c1��v1______v2��K1_____K3��p2____2p3����1(SO2)_____��3(SO2)����2(SO3)����3(SO2)_______1
����Ŀ���±���Ԫ�����ڱ�ǰ�����ڵ�һ���֣�X��Y��Z��R��W��J��6��Ԫ�صĴ��š�����JΪ0��Ԫ�ء�
X | Y | Z | |
R | |||
W | |||
J |
����˵����ȷ���ǣ� ��
A.��̬Rԭ�ӵĹ����ʾʽΪ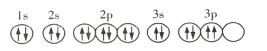
B.![]() ��
��![]() �İ뾶��С��ϵΪ
�İ뾶��С��ϵΪ![]()
C.Y�ĵ�һ�����ܴ���X�ĵ�һ������
D.X��Y��Z��R��W�У��縺������Ԫ��ΪW