题目内容
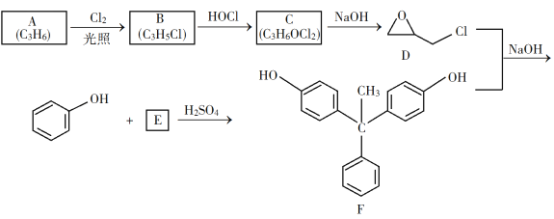
【题目】环氧树脂因其具有良好的机械性能、绝缘性能以及与各种材料的粘结性能,已广泛应用于涂料和胶黏剂等领域。下面是制备一种新型环氧树脂G的合成路线:

已知以下信息:
①
② ③
③
回答下列问题:
(1)A是一种烯烃,化学名称为__________,C中官能团的名称为_________、_________。
(2)由B生成C的反应类型为_________。
(3)由C生成D的反应方程式为__________________。
(4)E的结构简式为__________________。
(5)E的二氯代物有多种同分异构体,请写出其中能同时满足以下条件的芳香化合物的结构简式__________、_________。
①能发生银镜反应;②核磁共振氢谱有三组峰,且峰面积比为3∶2∶1。
(6)假设化合物D、F和![]() 恰好完全反应生成
恰好完全反应生成![]() 单一聚合度的G,若生成的
单一聚合度的G,若生成的![]() 和
和![]() 的总质量为
的总质量为![]() ,则G的n值理论上应等于__________。
,则G的n值理论上应等于__________。
【答案】丙烯 氯原子 羟基 加成反应 ![]() +NaOH→
+NaOH→![]() +NaCl+H2O或
+NaCl+H2O或![]() +NaOH→
+NaOH→![]() +NaCl+H2O
+NaCl+H2O 

 8
8
【解析】
A为烯烃,则A的结构简式为![]() ,在Cl2、光照条件下发生甲基上的取代反应生成ClCH2CH=CH2,C为饱和有机化合物,则B与HOCl发生加成反应,C结构中的-OH和-Cl原子在碱性条件下脱去HCl生成D,由于B与HOCl加成时-OH和-Cl的位置不确定,故C可能存在两种结构简式:
,在Cl2、光照条件下发生甲基上的取代反应生成ClCH2CH=CH2,C为饱和有机化合物,则B与HOCl发生加成反应,C结构中的-OH和-Cl原子在碱性条件下脱去HCl生成D,由于B与HOCl加成时-OH和-Cl的位置不确定,故C可能存在两种结构简式: ,
,![]() ,由F的结构简式可知,F由2份苯酚与1份E发生加成反应得到,反应机理是信息①,故E中含-C=O,发生的是加成反应,故E结构简式为:
,由F的结构简式可知,F由2份苯酚与1份E发生加成反应得到,反应机理是信息①,故E中含-C=O,发生的是加成反应,故E结构简式为: ,以此解答。
,以此解答。
(1)根据已知,A是烯烃,故A为![]() ,化学名称为丙烯;C为
,化学名称为丙烯;C为 或
或![]() ,所含官能团的名称为氯原子、羟基;
,所含官能团的名称为氯原子、羟基;
(2)依据A的结构简式,推测B中含有双键,依C的分子式可得C的不饱和度为0,故B和HOCl发生加成反应生成C;
(3)由C生成D的反应方程式为:![]() +NaOH→
+NaOH→![]() +NaCl+H2O或
+NaCl+H2O或![]() +NaOH→
+NaOH→![]() +NaCl+H2O;
+NaCl+H2O;
(4)由上述分析可知, E结构简式为: ;
;
(5)E的二氯代物有多种同分异构体,同时满足以下条件的芳香化合物;①能发生银镜反应,说明含有醛基;②核磁共振氢谱有三组峰,且峰面积比为3:2:1,说明分子中有3种类型的氢原子,且个数比为3:2:1,则符合条件的有机物的结构简式为 ;
; ;
;
(6)根据信息②和③,每消耗1molD,生成1molNaCl和1molH2O,若生成的NaCl和H2O的总质量为765g,生成NaCl和H2O的物质的量分别为![]() =10mol,由G的结构可知,要生成1mol单一聚合度的G,需要(n+2)molD,则(n+2)=10,解得n=8,即G的n值理论上应等于8。
=10mol,由G的结构可知,要生成1mol单一聚合度的G,需要(n+2)molD,则(n+2)=10,解得n=8,即G的n值理论上应等于8。

 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案【题目】下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素。

试回答下列问题:
(1)h的单质在空气中燃烧发出耀眼的白光,请用原子结构的知识解释发光的原因:_____ 。
(2)o、p两种元素的部分电离能数据如下表所示:
元素 | o | p | |
电离能/ |
| 717 | 763 |
| 1509 | 1561 | |
| 3248 | 2957 | |
比较两元素的![]() 、
、![]() 可知,气态
可知,气态![]() 再失去一个电子比气态
再失去一个电子比气态![]() 再失去一个电子难。对此,你的解释是 ___________。
再失去一个电子难。对此,你的解释是 ___________。
(3)表中所列的某主族元素的电离能情况如图所示,则该元素是上述元素中的____(填元素符号)。





