ЬтФПФкШн
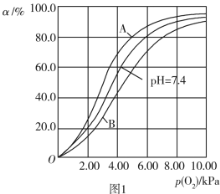
ЁОЬтФПЁПЬМЪЧЩњУќЕФЛљДЁЃЌНќМИФъПЦбЇМвУЧЗзЗзЯЦЦ№СЫбаОПЬМЕФШШГБЁЃЛиД№ЯТСаЮЪЬтЃК
ЃЈ1ЃЉ2019ФъШЫУЧЁАЬИіВЩЋБфЁБЃЌЦћГЕЮВЦјЪЧЮэіВЕФзяП§жЎвЛЁЃЦћГЕЮВЦјОЛЛЏЕФдРэЮЊЃК2NO(g)+2CO(g)=2CO2(g)+N2(g) ІЄHЃМ0ЁЃ
ФГЮТЖШЯТЃЌКуШнЕФУмБеШнЦїжаЭЈШыNOКЭCOЃЌВтЕУВЛЭЌЪБМфЕФNOКЭCOЕФХЈЖШШчЯТБэЃК
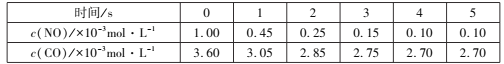
Ђй2sФкгУN2БэЪОЕФЛЏбЇЗДгІЫйТЪЮЊ___ЃЌИУЮТЖШЯТЃЌЗДгІЕФЛЏбЇЦНКтГЃЪ§ЮЊ___ЁЃ
ЂкШєИУЗДгІдкОјШШЁЂКуШнЕФУмБеЬхЯЕжаНјааЃЌЯТСаЪОвтЭМе§ШЗЧвФмЫЕУїЗДгІдкНјааЕНt1ЪБПЬДяЕНЦНКтзДЬЌЕФЪЧ___(ЬюДњКХ)ЁЃ
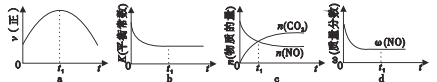
ЃЈ2ЃЉгУCH4ДпЛЏЛЙдNOxвВПЩвдМѕЩйЕЊЕФЮлШОЁЃ
вбжЊЃКCH4(g)+2NO2(g)= CO2(g)+ N2(g)+2H2O(g) ІЄH=867kJ/mol
2NO2(g)=N2O4(g) ІЄH=-56.9kJ/mol
H2O(g)=H2O(l) ІЄH=-44.0kJ/mol
аДГіCH4ДпЛЏЛЙдN2O4(g)ЩњГЩN2КЭH2OЃЈ1ЃЉЕФШШЛЏбЇЗНГЬЪНЃК___ЁЃ
ЃЈ3ЃЉГЃЮТГЃбЙЯТЃЌВтЕУЯђЫЎжаЭЈШызуСПЕФCO2КѓЃЌЫЎШмвКЕФpH=5.6ЁЃ
ЂйШєКіТдЫЎЕФЕчРыМАH2CO3ЕФЕкЖўМЖЕчРыЃЌдђH2CO3![]() HCO3-+H+ЕФЦНКтГЃЪ§KДѓдМЮЊ___ЁЃ(вбжЊЃКШмвКжаc(H2CO3)=1.5ЁС10-5 molL1ЃЌ10-5.6=2.5ЁС10-6)
HCO3-+H+ЕФЦНКтГЃЪ§KДѓдМЮЊ___ЁЃ(вбжЊЃКШмвКжаc(H2CO3)=1.5ЁС10-5 molL1ЃЌ10-5.6=2.5ЁС10-6)
ЂкГЃЮТЯТЃЌВтЕУNaHCO3ШмвКГЪМюадЃЌдђШмвКжаc(H2CO3)___c(CO32-)(ЬюЁА>ЁБЁАЁБЛђЁА<ЁБ)ЃЌдвђЪЧ___ (гУРызгЗНГЬЪНКЭБивЊЕФЮФзжЫЕУї)ЁЃ
ЂлЙјТЏжаЕФCaSO4ГСЕэПЩгУПЩШмадЬМЫсбЮНўШЁЃЌШЛКѓМгЫсГ§ШЅЃЌНўШЁЙ§ГЬжаЛсЗЂЩњЗДгІЃКCaSO4(s)+CO32-(aq)![]() CaCO3(s)+SO42-(aq)ЁЃ
CaCO3(s)+SO42-(aq)ЁЃ
вбжЊ298KЪБЃЌKsp(CaCO3)=2.80ЁС10-9ЃЌKsp(CaSO4)=4.90ЁС10-5ЃЌдђДЫЮТЖШЯТИУЗДгІЕФЦНКтГЃЪ§KЮЊ___(МЦЫуНсЙћБЃСєШ§ЮЛгааЇЪ§зж)ЁЃ
ЁОД№АИЁП1.875ЁС104 molL1s1 5000 bd CH4(g) + N2O4 (g) = CO2(g)+N2(g)+2H2O(l) ІЄH= 898.1 kJЁЄmol1 4.2ЁС107 molL1 > ЬМЫсЧтФЦШмвКжаДцдкЫЎНтЦНКтHCO3Ѓ+H2O![]() H2CO3 + OHЃКЭЕчРыЦНКтHCO3Ѓ
H2CO3 + OHЃКЭЕчРыЦНКтHCO3Ѓ![]() CO32+H+ЃЌЫЎНтГЬЖШДѓгкЕчРыГЬЖШЃЌШмвКЯдМюад 1.75ЁС104
CO32+H+ЃЌЫЎНтГЬЖШДѓгкЕчРыГЬЖШЃЌШмвКЯдМюад 1.75ЁС104
ЁОНтЮіЁП
ЂХЂйЯШМЦЫуЧА2sФкЕФІЄc(NO)ЃЌдйМЦЫуІЄc(N2)КЭЦНОљЗДгІЫйТЪЃЌЯШМЦЫуЦНКтЪБУПИіЮяжЪЕФХЈЖШЃЌдйМЦЫуЦНКтГЃЪ§ЁЃ
Ђкa. ЗДгІДяЕНЦНКтЪБЃЌИїЮяжЪЕФЫйТЪВЛдйИФБфЃЛb. ОјШШШнЦїжаЃЌЗДгІЗХШШЃЌЮТЖШЩ§ИпЃЌЦНКтГЃЪ§МѕаЁЃЌЕБЦНКтГЃЪ§МѕаЁЕНВЛИФБфЪБЃЌдђДяЕНЦНКтЃЛc. етСНепЕФЮяжЪЕФСПЯрЕШВЛвЛЖЈФмЫЕУїДяЕНЦНКтЃЌжЛгаетСНепЕФЮяжЪЕФСПВЛдйИФБфЃЌдђДяЕНЦНКтЃЛd. жЪСПЗжЪ§ВЛдйИФБфЃЌдђДяЕНЦНКтЁЃ
ЂЦЕквЛИіЗНГЬЪНМѕШЅЕкЖўИіЗНГЬЪНдйМгЕкШ§ИіЗНГЬЪНЕФ2БЖЁЃ
ЂЧИљОнЕчРыЦНКтМЦЫуЦНКтГЃЪ§ЃЛЂкГЃЮТЯТЃЌВтЕУNaHCO3ШмвКГЪМюадЃЌжївЊдвђЪЧЬМЫсЧтФЦШмвКжаДцдкЫЎНтЦНКтHCO3Ѓ+H2O![]() H2CO3 + OHЃКЭЕчРыЦНКтHCO3Ѓ
H2CO3 + OHЃКЭЕчРыЦНКтHCO3Ѓ![]() CO32+H+ЃЌЫЎНтГЬЖШДѓгкЕчРыГЬЖШЃЌШмвКЯдМюадЃЛЂлНўШЁЙ§ГЬжаЛсЗЂЩњЗДгІЃКCaSO4(s)+CO32 (aq)
CO32+H+ЃЌЫЎНтГЬЖШДѓгкЕчРыГЬЖШЃЌШмвКЯдМюадЃЛЂлНўШЁЙ§ГЬжаЛсЗЂЩњЗДгІЃКCaSO4(s)+CO32 (aq)![]() CaCO3(s)+SO42 (aq)ЃЌИљОнЦНКтГЃЪ§КЭШмЖШЛ§ГЃЪ§НјааМЦЫуЁЃ
CaCO3(s)+SO42 (aq)ЃЌИљОнЦНКтГЃЪ§КЭШмЖШЛ§ГЃЪ§НјааМЦЫуЁЃ
ЂХЂйЧА2sФкЕФІЄc(NO) =(1.00Ѓ0.25)ЁС103 molЁЄL1 =7.50ЁС104 molЁЄL1ЃЌдђІЄc(N2) = ![]() ЁС7.50ЁС104 molЁЄL1=3.75ЁС104 molЁЄL1ЃЌЦНОљЗДгІЫйТЪ
ЁС7.50ЁС104 molЁЄL1=3.75ЁС104 molЁЄL1ЃЌЦНОљЗДгІЫйТЪ![]() ЃЛЗДгІДяЕНЦНКтЪБc(CO) =1ЁС104 molЁЄL1ЃЌc(NO)= 2.7ЁС103 molЁЄL1ЃЌc(N2) =ІЄc(N2) =
ЃЛЗДгІДяЕНЦНКтЪБc(CO) =1ЁС104 molЁЄL1ЃЌc(NO)= 2.7ЁС103 molЁЄL1ЃЌc(N2) =ІЄc(N2) = ![]() ЁС9ЁС104 molЁЄL1=4.5ЁС104 molЁЄL1ЃЌдђc(CO2) =ІЄc(CO2) =ІЄc(CO)= 9ЁС104 molЁЄL1ЃЌИУЮТЖШЯТЃЌЗДгІЕФЛЏбЇЦНКтГЃЪ§ЮЊ
ЁС9ЁС104 molЁЄL1=4.5ЁС104 molЁЄL1ЃЌдђc(CO2) =ІЄc(CO2) =ІЄc(CO)= 9ЁС104 molЁЄL1ЃЌИУЮТЖШЯТЃЌЗДгІЕФЛЏбЇЦНКтГЃЪ§ЮЊ![]() ЃЛЙЪД№АИЮЊЃК1.875ЁС104 molL1s1ЃЛ5000ЁЃ
ЃЛЙЪД№АИЮЊЃК1.875ЁС104 molL1s1ЃЛ5000ЁЃ
Ђкa. ЗДгІДяЕНЦНКтЪБЃЌИїЮяжЪЕФЫйТЪВЛдйИФБфЃЌЙЪaВЛЗћКЯЬтвтЃЛb. ОјШШШнЦїжаЃЌЗДгІЗХШШЃЌЮТЖШЩ§ИпЃЌЦНКтГЃЪ§МѕаЁЃЌЕБЦНКтГЃЪ§МѕаЁЕНВЛИФБфЪБЃЌдђДяЕНЦНКтЃЌЙЪbЗћКЯЬтвтЃЛc. етСНепЕФЮяжЪЕФСПЯрЕШВЛвЛЖЈФмЫЕУїДяЕНЦНКтЃЌжЛгаетСНепЕФЮяжЪЕФСПВЛдйИФБфЃЌдђДяЕНЦНКтЃЌЙЪcВЛЗћКЯЬтвтЃЛd. жЪСПЗжЪ§ВЛдйИФБфЃЌдђДяЕНЦНКтЃЌЙЪdЗћКЯЬтвтЃЛзлЩЯЫљЪіЃЌД№АИЮЊbdЁЃ
ЂЦЕквЛИіЗНГЬЪНМѕШЅЕкЖўИіЗНГЬЪНдйМгЕкШ§ИіЗНГЬЪНЕФ2БЖЃЌМДЕУCH4ДпЛЏЛЙдN2O4(g)ЩњГЩN2КЭH2O(l)ЕФШШЛЏбЇЗНГЬЪНЃКCH4(g) + N2O4 (g) = CO2(g)+N2(g)+2H2O(l) ІЄH= 867 kJЁЄmol1(56.9 kJЁЄmol1) +2ЁС(44 kJЁЄmol1) = 898.1 kJЁЄmol1ЃЛЙЪД№АИЮЊЃКCH4(g) + N2O4 (g) = CO2(g)+N2(g)+2H2O(l) ІЄH= 898.1 kJЁЄmol1ЁЃ
ЂЧЂйКіТдЫЎЕФЕчРыМАH2CO3ЕФЕкЖўМЖЕчРыЃЌдђH2CO3![]() HCO3Ѓ+H+ЕФЦНКтГЃЪ§KДѓдМЮЊ
HCO3Ѓ+H+ЕФЦНКтГЃЪ§KДѓдМЮЊ ЃЛЙЪД№АИЮЊЃК4.2ЁС107 molL1ЁЃ
ЃЛЙЪД№АИЮЊЃК4.2ЁС107 molL1ЁЃ
ЂкГЃЮТЯТЃЌВтЕУNaHCO3ШмвКГЪМюадЃЌдвђЪЧЬМЫсЧтФЦШмвКжаДцдкЫЎНтЦНКтHCO3Ѓ+H2O![]() H2CO3 + H+КЭЕчРыЦНКтHCO3Ѓ
H2CO3 + H+КЭЕчРыЦНКтHCO3Ѓ![]() CO32+H+ЃЌЫЎНтГЬЖШДѓгкЕчРыГЬЖШЃЌШмвКЯдМюадЃЌвђДЫШмвКжаc(H2CO3) >c(CO32)ЃЛЙЪД№АИЮЊЃК>ЃЛЬМЫсЧтФЦШмвКжаДцдкЫЎНтЦНКтHCO3Ѓ+H2O
CO32+H+ЃЌЫЎНтГЬЖШДѓгкЕчРыГЬЖШЃЌШмвКЯдМюадЃЌвђДЫШмвКжаc(H2CO3) >c(CO32)ЃЛЙЪД№АИЮЊЃК>ЃЛЬМЫсЧтФЦШмвКжаДцдкЫЎНтЦНКтHCO3Ѓ+H2O![]() H2CO3 + OHЃКЭЕчРыЦНКтHCO3Ѓ
H2CO3 + OHЃКЭЕчРыЦНКтHCO3Ѓ![]() CO32+H+ЃЌЫЎНтГЬЖШДѓгкЕчРыГЬЖШЃЌШмвКЯдМюадЁЃ
CO32+H+ЃЌЫЎНтГЬЖШДѓгкЕчРыГЬЖШЃЌШмвКЯдМюадЁЃ
ЂлНўШЁЙ§ГЬжаЛсЗЂЩњЗДгІЃКCaSO4(s)+CO32 (aq)![]() CaCO3(s)+SO42 (aq)ЃЌ
CaCO3(s)+SO42 (aq)ЃЌ
 ЃЛЙЪД№АИЮЊЃК1.75ЁС104ЁЃ
ЃЛЙЪД№АИЮЊЃК1.75ЁС104ЁЃ

 дФЖСПьГЕЯЕСаД№АИ
дФЖСПьГЕЯЕСаД№АИЁОЬтФПЁПЯТЭМЪЧРћгУЗЯЭаМЃЈКЌдгжЪЬњЃЉжЦБИЕЈЗЏЃЈСђЫсЭОЇЬхЃЉЕФСїГЬЁЃ

ВПЗжбєРызгвдЧтбѕЛЏЮяаЮЪНГСЕэЪБШмвКЕФpHМћЯТБэЃК
ГСЕэЮя | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 |
ПЊЪМГСЕэ | 2.7 | 7.5 | 4.4 |
ЭъШЋГСЕэ | 3.7 | 9.7 | 6.7 |
ЧыЛиД№ЃК
ЃЈ1ЃЉШмвКBжаКЌгаЕФбєРызгга____________________ЃЈЬюРызгЗћКХЃЉЁЃ
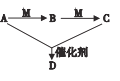
ЃЈ2ЃЉЯТСаЮяжЪжазюЪЪвЫзібѕЛЏМСXЕФЪЧ__________ЃЈЬюзжФИЃЉЁЃ
aЃЎNaClO bЃЎH2O2 cЃЎKMnO4
ЃЈ3ЃЉМгШыЪдМСЂйЪЧЮЊСЫЕїНкpHЃЌвЊЕїећpHЗЖЮЇЪЧ_____________ЃЌдђЪдМСЂйПЩвдбЁдё______________ЃЈЬюЛЏбЇЪНЃЉЁЃ
ЃЈ4ЃЉГСЕэDМгШыбЮЫсКЭЬњЗлЃЌПЩвджЦЕУFeCl2ШмвКЃЌЪЕбщЪвБЃДцFeCl2ШмвКЃЌашМгШыЙ§СПЕФЬњЗлЃЌЦфдвђЪЧ____________________________________ЃЈгУРызгЗНГЬЪНБэЪОЃЉЁЃ
ЃЈ5ЃЉШмвКEОЙ§ВйзїЂйПЩЕУЕНЕЈЗЏЃЌВйзїЂйЮЊ________________________ЁЂЙ§ТЫЁЂЯДЕгЁЃ
ЃЈ6ЃЉвбжЊШмвКжаcЃЈCu2+ЃЉгыpHЕФЙиЯЕЮЊlgcЃЈCu2+ЃЉ=8.6-2pHЃЌШєШмвКжаcЃЈCu2+ЃЉЮЊ1mol/LЃЌДЫЪБШмвКжаЕФFe3+ФмЗёГСЕэЭъШЋЃК___________ЃЈЬюЁАФмЁБЛђЁАЗёЁБЃЉ ЁЃ