题目内容
12.某有机物分子式为C4H8,据此推测其结构和性质不可能的是( )| A. | 含有3个甲基 | B. | 一氯代物只有一种 | ||
| C. | 使溴水褪色 | D. | 四个碳原子共平面 |
分析 A.若含有3个甲基,分子中H原子数目大于8;
B.该有机物可能为环丁烷;
C.该有机物可能为丁烯;
D.该有机物可能为CH3CH=CHCH3或CH2=C(CH3)2.
解答 解:A.若含有3个甲基,分子中H原子数目大于8,故不可能含有3个甲基,故A错误;
B.该有机物可能为环丁烷,分子中只有一种H原子,一氯代物只有一种,故B正确;
C.该有机物可能为丁烯,含有碳碳双键,能与溴发生加成反应,使溴水褪色,故C正确;
D.该有机物可能为CH3CH=CHCH3或CH2=C(CH3)2,碳碳双键为平面结构,所有碳原子处于同一平面,故D正确,
故选:A.
点评 本题考查有机物的结构与性质,关键是根据分子式判断物质可能的结构,难度不大,有利于学生发散思维培养.

练习册系列答案
 一课四练系列答案
一课四练系列答案 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案 新辅教导学系列答案
新辅教导学系列答案 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案
相关题目
2.A、B、C、D、E为原子序数依次增大的短周期主族元素,A原子的最外层电子数为内层电子数的2倍,B原子的M电子层有1个电子,C的氢氧化物既能与强酸反应又能与强碱反应,D的最高正价和最低负价的代数和为4,E在同周期主族元素中原子半径最小.下列叙述错误的是( )
| A. | 元素C位于周期表中第三周期ⅢA族 | |
| B. | 熔融电解化合物CE3可制取单质C | |
| C. | D的最高价含氧酸的浓溶液与单质A共热时能生成三种氧化物 | |
| D. | 化合物B2D2中既含离子键又含非极性共价键 |
3.下列叙述中,正确的是( )
| A. | 强电解质的导电性一定比弱电解质的导电性强 | |
| B. | 溶解度小的物质的导电性一定比溶解度大的物质的导电性弱 | |
| C. | 金属元素从化合态变为游离态时,该元素一定被还原 | |
| D. | 金属阳离子得电子多时氧化性强 |
20.下列反应的离子方程式书写正确的是( )
| A. | NaHCO3溶液中和盐酸:CO${\;}_{{3}_{\;}}$2-+2H+=H2O+CO2↑ | |
| B. | 用稀硝酸洗涤试管内壁的银镜:Ag+2H++NO3-=Ag++NO↑+H2O | |
| C. | 向碳酸氢铵溶液中加过量的NaOH溶液并加热:NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O | |
| D. | 用MnS除去MnCl2溶液中的Cu2+:MnS+Cu2+=CuS+Mn2+ |
7.V L含有(NH4)2SO4和K2SO4的混合溶液,已知NH4+浓度为amol•L-1,SO42-浓度为bmol•L-1.则原混合溶液中钾离子的物质的量浓度为( )
| A. | (b-2a)bmol•L-1 | B. | $\frac{(b-2a)}{2}$bmol•L-1 | C. | (2b-a)bmol•L-1 | D. | $\frac{(2b-a)}{2}$bmol•L-1 |
17.将c mol/L的AlCl3溶液V1mL加水稀释至V2mL,稀释后溶液中Cl-物质的量浓度为 ( )
| A. | c mol/L | B. | 3c mol/L | C. | $\frac{3c{V}_{1}}{{V}_{2}}$mol/L | D. | $\frac{c{V}_{1}}{{V}_{2}}$mol/L |
4.下列有关化学用语的表示正确的是( )
| A. | 四氯化碳分子的电子式: | B. | 对硝基甲苯的结构简式: | ||
| C. | 羟基的电子式: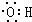 | D. | 乙醛的结构简式:CH3COH |