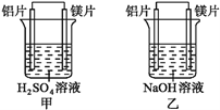
��Ŀ����
����Ŀ����ҵ������þ��(��Ҫ�ɷ�ΪMgCO3��������FeCO3)Ϊԭ���Ʊ�����þ��ʵ���������£�
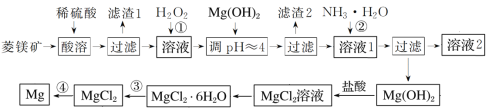
��֪��һЩ��������ת��Ϊ�����������ʱ��Һ��pH�����ʾ
Fe3+ | Al3+ | Fe2+ | Mg2+ | |
��ʼ����ʱ | 1.5 | 3.3 | 6.5 | 9.4 |
��ȫ����ʱ | 3.7 | 5.2 | 9.7 |
��ش�
(1)���û�й��̢٣�����ǣ�__________________________________��
(2)���������б�ѭ��ʹ�õ������ǣ�____________��
(3)����2����Ҫ�ɷ�Ϊ��____________����Һ2�е���Ҫ����Ϊ��_____________��
(4)ͨ����Ϊ��������Һ�е�����Ũ��С��1��10-5 mol��L-1ʱ����Ϊ������ȫ��Ϊ��֤Mg2+������ȫ�����̢��п�����Һ��pH����Ϊ________��(����С�����һλ)(��֪Mg(OH)2��Ksp=2��10-11��lg2=0.3)
(5)��֪MgCl2��6H2O����ʱ����ˮ�⣺MgCl2��6H2O=Mg(OH)Cl+HCl��+5H2O�����̢�Ӧ����β������ܵõ���ˮMgCl2����_______________________________________________��
(6)д�����̢��з�����Ӧ�Ļ�ѧ����ʽ��_____________________________________��
(7)Ϊ�ⶨ��þ�������ĺ�������ȡ12.5 g��þ����Ʒ���ڹ�����ϡ���Ტ��ȫת�Ƶ���ƿ�У���0.010 mol��L��1H2O2��Һ���еζ���ƽ�вⶨ4�飬����H2O2��Һ��������ݼ�¼���±���ʾ��
ʵ���� | 1 | 2 | 3 | 4 | ƽ��ֵ |
����H2O2��Һ�����/mL | 15.00 | 15.02 | 15.62 | 14.98 |
�ٸ��ݱ������ݣ��ɼ������������������������Ϊ__________%��(������λС��)
��H2O2��ҺӦװ��__________ �ζ�����(������ʽ��������ʽ��)
�����
a�������������������ζ��յ�ʱ���Ӷ����ᵼ��������_________��
b���ζ�֮ǰû���ų��ζ��е����ݻᵼ��������_________��
���𰸡�����ȥFe2+ Mg(OH)2 Fe(OH)3 (NH4)2SO4 11.2 �ڸ����Ȼ����������������¼��ȷֽ� MgCl2(����)![]() Mg+Cl2�� 0.13 ��ʽ ƫ�� ƫ��
Mg+Cl2�� 0.13 ��ʽ ƫ�� ƫ��
��������
(1)���̢����ù��������Fe2+����ΪFe3+��ͨ������pH=4��������������������(2)��������ͼ��������ѭ��ʹ�õ�������(3)����һЩ��������ת��Ϊ�����������ʱ��Һ��pH������pH=4��Fe3+������ȫ��������������������Һ1����Ҫ�ɷ�������þ�����백ˮ����������þ����������泥�(4)����Mg(OH)2���ܶȻ��������� c(Mg2+)=1��10-5 mol��L-1ʱ��c(OH-)��ֵ��(5) Ҫ�õ���ˮMgCl2��Ҫ����MgCl2ˮ����(6���̢��ǵ�������Ȼ�þ����þ��������(7) �� ����![]() ��������������������H2O2��Һ���������ԣ��۸���
��������������������H2O2��Һ���������ԣ��۸���![]() ���������
���������
��1�����̢����ù��������Fe2+����ΪFe3+��ͨ������pH=4�����������������������û�й��̢٣�����ȥFe2+��(2)��������ͼ����ѭ��ʹ�õ�������Mg(OH)2��(3)����һЩ��������ת��Ϊ�����������ʱ��Һ��pH������pH=4��Fe3+������ȫ��������������������������2����Ҫ�ɷ�ΪFe(OH)3����Һ1����Ҫ�ɷ�������þ�����백ˮ����������þ����������泥����˺�õ�����Һ2������Ҫ����Ϊ(NH4)2SO4��(4)����Mg(OH)2���ܶȻ���������c(Mg2+)![]() c2(OH-)=2��10-11�� c(Mg2+)=1��10-5 mol��L-1ʱ��c(OH-)=
c2(OH-)=2��10-11�� c(Mg2+)=1��10-5 mol��L-1ʱ��c(OH-)=![]() ��c(H+)=
��c(H+)=![]() ��pH=-
��pH=-![]() (
( ![]() =11.2�����Թ��̢��п�����Һ��pH����Ϊ11.2��(5) �ڸ����Ȼ����������������¼��ȷֽ�MgCl2��6H2O�����ܵõ���ˮMgCl2��(6)���̢��ǵ�������Ȼ�þ����þ����������Ӧ����ʽ��MgCl2(����)
=11.2�����Թ��̢��п�����Һ��pH����Ϊ11.2��(5) �ڸ����Ȼ����������������¼��ȷֽ�MgCl2��6H2O�����ܵõ���ˮMgCl2��(6)���̢��ǵ�������Ȼ�þ����þ����������Ӧ����ʽ��MgCl2(����)![]() Mg+Cl2����(7)��ʵ��3���ϴ�������㣬����H2O2��Һ�����ƽ��ֵΪ15.00mL������������������������Ϊx��
Mg+Cl2����(7)��ʵ��3���ϴ�������㣬����H2O2��Һ�����ƽ��ֵΪ15.00mL������������������������Ϊx��
![]()
112g 1mol
12.5x g 0.010 mol��L��1![]() 0.015L
0.015L
![]()
X=0.13%
��H2O2��Һ���������ԣ�Ӧװ����ʽ�ζ���������a�������������������ζ��յ�ʱ���Ӷ��������ı�Һ���ƫ�����ᵼ��������ƫ����b���ζ�֮ǰû���ų��ζ��е����������ı�Һ���ƫ�����ᵼ��������ƫ�ߡ�

����Ŀ��ͭ������(��Ҫ����ͭ����������������)����ɫ����������������Ҫ�ġ�������Դ�����������������ʵ����Դ���ۺ����þ�����Ҫ���塣һ�ִ�ͭ�������з�����ȡ���ֽ���Ԫ�صĹ�����������
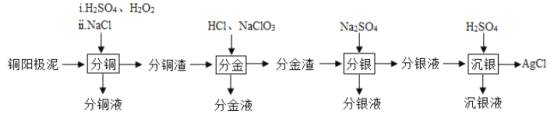
��֪:�ֽ�Һ����Ҫ�ɷ�Ϊ[AuCl4]��;�ֽ�������Ҫ�ɷ�ΪAgCl;����Һ����Ҫ�ɷ�ΪAg(SO3)2]3�����Ҵ���[Ag(SO3)2]3��![]() Ag++2SO32��
Ag++2SO32��
(1)����ͭ��ʱ������ͭ������Ӧ�Ļ�ѧ����ʽΪ_______________________����֪����ͭ��ʱ��Ԫ�صĽ��������±���ʾ��
Cu | Au | Ag | Ni | |
������% | 85.7 | 0 | 4.5 | 93.5 |
����ͭ��ʱ����������NaC1����Ҫ����Ϊ_________________________________��
(2)���ֽ���ʱ�����ʽ�����Ӧ�����ӷ���ʽΪ__________________________��
(3)ijС��ģ�ҵ�ϻ��շ������е�������������:
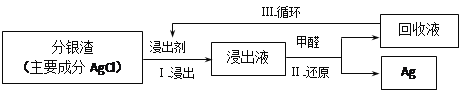
����Ҫ��Ӧ:AgCl+2SO32��![]() Ag(SO3)23��+C1��
Ag(SO3)23��+C1��
���о�����:������������ʱ���÷�Ӧ�ڳ��������н��У�����ʱ�������ʹ���Ľ�����(����Һ����������ռ��ʼ�����������������İٷֱ�)���ͣ�����ԭ����____________________��
�������з�Ӧ�����ӷ���ʽ��������:
_____Ag(SO3)23-+_____OH��+_____==_____+_____SO32��+_____+CO32��
���л���Һ��ֱ��ѭ��ʹ�ã���ѭ����κ����Ľ����ʻή�͡��ӻ���Һ����Ũ�ȱ仯�ͷ�Ӧ�ȵĽǶȷ���ԭ��:________________________________________��
(4)��ҵ�ϣ�������⾫��ʱ���������Һ��pHΪ1.5��2������Ϊ5��10A������7A�ĵ������60min�õ�21.6gAg����õ��صĵ��Ч��Ϊ________%��(����С�����λ��ͨ��һ�������ʱ������ʵ�ʳ����Ľ���������������Ӧ�����Ľ�������֮�Ƚе��Ч�ʡ������ڳ���Ϊ96500C��mol��1)