籾朕坪否
‐籾朕/和双傍隈嶄⇧辛參屬苧郡哘N2⇦3H2![]() 2NH3厮器欺峠財彜蓑議頁( )
2NH3厮器欺峠財彜蓑議頁( )
〙1倖N《N囚僅叢議揖扮嗤3倖H!H囚侘撹
〖N2、H2、NH3議蛍徨方岻曳葎1|3|2
〗1倖N《N囚僅叢議揖扮嗤6倖N!H囚侘撹
∠N2、H2、NH3議敵業音壅延晒
A. 〙∠ B. 〖〗 C. 〙〗 D. 〖∠
‐基宛/A
‐盾裂/
辛剃郡哘議峠財彜蓑登僅卆象頁^延楚音延 ̄匯協峠財。
〙.喇圭殻塀辛岑⇧耽僅叢1倖N《N議揖扮⇧匯協嗤3倖H-H囚僅叢⇧飛揖扮嗤3倖H-H侘撹⇧夸傍苧v屎=v剃⇧晒僥郡哘器欺峠財彜蓑⇧絞〙僉◉
〖.籾孤隆御岑光麗嵎議軟兵楚參式廬晒楕⇧涙隈登僅器欺峠財扮N2、H2、NH3議蛍徨方岻曳⇧絞功象蛍徨倖方曳涙隈登僅郡哘頁倦器欺峠財彜蓑⇧絞〖音僉◉
〗.喇圭殻塀辛岑⇧耽僅叢1倖N《N⇧匯協氏嗤6倖N-H囚侘撹⇧絞涙隈登僅頁倦器欺峠財彜蓑⇧絞〗音僉◉
∠.輝凪万訳周音延⇧郡哘嶄麗嵎議敵業音壅延晒扮⇧郡哘匯協器欺峠財彜蓑⇧絞∠僉◉忝貧侭峰⇧辛參屬苧乎郡哘厮器欺峠財彜蓑議頁〙∠⇧絞基宛葎A。

 仟試薦悳強埀菩狼双基宛
仟試薦悳強埀菩狼双基宛 霜繁夕慕酔赤邪豚菩邪恬匍孱巒寄僥竃井芙狼双基宛
霜繁夕慕酔赤邪豚菩邪恬匍孱巒寄僥竃井芙狼双基宛‐籾朕/垢匍貧參曹綻嵩(麼勣撹蛍葎MgCO3⇧根富楚FeCO3)葎圻創崙姥署奉綻議糞刮送殻泌和⦿
厮岑⦿匯乂署奉宣徨廬晒葎狽剳晒麗柿牛扮卑匣議pH泌燕侭幣
Fe3+ | Al3+ | Fe2+ | Mg2+ | |
蝕兵柿牛扮 | 1.5 | 3.3 | 6.5 | 9.4 |
頼畠柿牛扮 | 3.7 | 5.2 | 9.7 |
萩指基⦿
(1)泌惚短嗤狛殻〙⇧朔惚頁⦿__________________________________。
(2)貧峰送殻嶄瓜儉桟聞喘議麗嵎頁⦿____________。
(3)陀奧2議麼勣撹蛍葎⦿____________◉卑匣2嶄議麼勣卑嵎葎⦿_____________。
(4)宥械範葎火藻壓卑匣嶄議宣徨敵業弌噐1〜10-5 mol,L-1扮祥範葎柿牛頼畠⇧葎隠屬Mg2+柿牛頼畠⇧狛殻〖嶄陣崙卑匣議pH崛富葎________。(隠藻弌方泣朔匯了)(厮岑Mg(OH)2議Ksp=2〜10-11⇧lg2=0.3)
(5)厮岑MgCl2,6H2O鞭犯扮窟伏邦盾⦿MgCl2,6H2O=Mg(OH)Cl+HCl●+5H2O⇧狛殻〗哘乎泌採荷恬嘉嬬誼欺涙邦MgCl2◦⦿_______________________________________________。
(6)亟竃狛殻∠嶄窟伏郡哘議晒僥圭殻塀⦿_____________________________________。
(7)葎霞協曹綻嵩嶄鑓議根楚。各函12.5 g曹綻嵩劔瞳卑噐狛楚議蓮葬磨旺頼畠廬卞欺弑侘匿嶄⇧喘0.010 mol,L!1H2O2卑匣序佩砧協。峠佩霞協4怏⇧嶧債H2O2卑匣議悶持方象芝村泌和燕侭幣。
糞刮園催 | 1 | 2 | 3 | 4 | 峠譲峙 |
嶧債H2O2卑匣議悶持/mL | 15.00 | 15.02 | 15.62 | 14.98 |
〙功象燕嶄方象⇧辛柴麻竃曹鑓嵩嶄鑓議嵎楚蛍方葎__________%。(隠藻曾了弌方)
〖H2O2卑匣哘廾壓__________ 砧協砿嶄(野^磨塀 ̄賜^珠塀 ̄)
〗列餓
a⤴凪万荷恬譲屎械⇧砧協嶮泣扮剿篇響方氏擬崑侭霞潤惚_________。
b⤴砧協岻念短嗤電茅砧協嶄議賑倒氏擬崑侭霞潤惚_________。
‐籾朕/蝶梁業扮⇧壓2L議畜液否匂嶄⇧X、Y、Z(譲葎賑悶)眉嶽麗嵎議楚昧扮寂議延晒爆㞍泌夕侭幣⦿
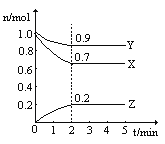
(1)喇夕嶄侭公方象序佩蛍裂⇧乎郡哘議晒僥圭殻塀葎__________。
(2)飛貧峰郡哘嶄X、Y、Z蛍艶葎H2、N2、NH3⇧蝶梁業和⇧壓否持冴協葎2.0L議畜液否匂嶄割秘2.0mol N2才2.0mol H2⇧匯粁扮寂朔郡哘器峠財彜蓑⇧糞刮方象泌燕侭幣⦿
t/s | 0 | 50 | 150 | 250 | 350 |
n(NH3) | 0 | 0.36 | 0.48 | 0.50 | 0.50 |
0~50s坪議峠譲郡哘堀楕v(N2)=__________。
(3)厮岑⦿囚嬬峺壓炎彈彜趨和⇧繍1mol賑蓑蛍徨AB(g)盾宣葎賑蓑圻徨A(g)、B(g)侭俶議嬬楚⇧喘憲催E燕幣⇧汽了葎kJ/mol。H-H議囚嬬葎436kJ/mol⇧N-H議囚嬬葎391kJ/mol⇧伏撹1mol NH3狛殻嶄慧竃46kJ議犯楚。夸N《N議囚嬬葎_________kJ/mol。