题目内容
实验室里迅速制备少量氯气可利用以下反应:2KMnO4+16HCl═2KCl+2MnCl2+5Cl2↑+8H2O此反应不需要加热,常温下就可以迅速进行,而且对盐酸的浓度要求不高.
(1)用“双线桥法”表示出电子转移情况:2KMnO4+16HCl═2KCl+2MnCl2+5Cl2↑+8H2O
(2)该反应中,氧化剂是 ,还原剂是 .
(3)当电子转移的数目为6.02×1023个时,求生成的氯气的物质的量和被氧化的HCl的质量.(写出计算过程)
(1)用“双线桥法”表示出电子转移情况:2KMnO4+16HCl═2KCl+2MnCl2+5Cl2↑+8H2O
(2)该反应中,氧化剂是
(3)当电子转移的数目为6.02×1023个时,求生成的氯气的物质的量和被氧化的HCl的质量.(写出计算过程)
考点:氧化还原反应
专题:氧化还原反应专题
分析:2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O中,Mn元素的化合价由+7价降低为+2价,Cl元素的化合价由-1价升高为0,该反应中转移10e-,以此来解答.
解答:
解:(1)Mn得到电子,Cl失去电子,该反应中转移10e-,“双线桥法”表示该反应电子转移的方向和数目为 ,
,
故答案为: ;
;
(2)Mn元素的化合价降低,Cl元素的化合价升高,则KMnO4为氧化剂,HCl为还原剂,故答案为:KMnO4;HCl;
(3)当电子转移的数目为6.02×1023个时,即转移1mol电子,生成的氯气的物质的量为1mol×
=0.5mol,由Cl原子守恒可知,被氧化的HCl的质量为0.5mol×2×36.5g/mol=36.5g,答:生成的氯气的物质的量为0.5mol,被氧化的HCl的质量为36.5g.
 ,
,故答案为:
 ;
;(2)Mn元素的化合价降低,Cl元素的化合价升高,则KMnO4为氧化剂,HCl为还原剂,故答案为:KMnO4;HCl;
(3)当电子转移的数目为6.02×1023个时,即转移1mol电子,生成的氯气的物质的量为1mol×
| 5 |
| 10 |
点评:本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重氧化还原反应基本概念及计算的考查,题目难度不大.

练习册系列答案
 激活思维优加课堂系列答案
激活思维优加课堂系列答案 活力试卷系列答案
活力试卷系列答案 课课优能力培优100分系列答案
课课优能力培优100分系列答案
相关题目
下列说法正确的是( )
| A、冰和干冰既是纯净物又是化合物 |
| B、蔗糖、硫酸钡和水分别属于非电解质、强电解质和弱电解质 |
| C、硫酸、纯碱、醋酸钠和生石灰分别属于酸、碱、盐和氧化物 |
| D、盐酸和食醋既是化合物又是酸 |
对于平衡:2A+2B?C+2D+3E+H2O(A、B、C、D、E为溶液中可自由移动的微粒),下列判断正确的是( )
| A、加水平衡左移 |
| B、增加A,可提高B的转化率 |
| C、平衡后,按起始投料比,再次投入A和B,则A和B的转化率都将增大 |
| D、升温该平衡一定发生移动 |
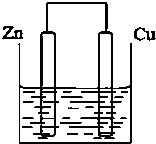 将质量相等的锌片和铜片用导线相连浸500mL硫酸铜溶液中构成如图的装置.
将质量相等的锌片和铜片用导线相连浸500mL硫酸铜溶液中构成如图的装置.