题目内容
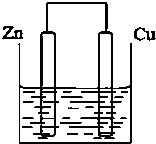 将质量相等的锌片和铜片用导线相连浸500mL硫酸铜溶液中构成如图的装置.
将质量相等的锌片和铜片用导线相连浸500mL硫酸铜溶液中构成如图的装置.(1)此装置为
(2)若2min后测得锌片质量减少1.3g,则导线中流过的电子为
考点:原电池和电解池的工作原理
专题:电化学专题
分析:(1)装置是否有外加电源可以判断所属的类别,根据Zn与铜离子的置换反应来书写;
(2)根据电极反应式来计算.
(2)根据电极反应式来计算.
解答:
解:(1)装置没有外加电源,属于原电池,活泼金属锌做负极,本身失电子,正极上是铜离子得电子,正极反应和负极反应合并即为总的电池反应,则该装置中发生反应总的离子方程式为Zn+Cu2+═Zn2++Cu;
故答案为:原电池;Zn+Cu2+═Zn2++Cu;
(2)根锌极发生的反应为:Zn-2e-→Zn2+,锌片质量减少1.3g,即减少0.02mol时,转移电子0.04mol,故答案为:0.04.
故答案为:原电池;Zn+Cu2+═Zn2++Cu;
(2)根锌极发生的反应为:Zn-2e-→Zn2+,锌片质量减少1.3g,即减少0.02mol时,转移电子0.04mol,故答案为:0.04.
点评:本题考查学生原电池的工作原理,注意把握电池方程式的书写方法,难度不大.

练习册系列答案
 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案
相关题目
关于物质的用途说法错误的是( )
| A、二氧化硅用于制造光导纤维 |
| B、聚氯乙烯塑料(PVC)可制成薄膜做食品包装材料 |
| C、可以用Si3N4、Al2O3制作高温结构陶瓷制品 |
| D、铝合金用于制造门窗 |
下列离子方程式书写正确的是( )
| A、铝粉投入到NaOH溶液中:2Al+2OH-═2AlO2-+H2↑ |
| B、AlCl3溶液中加入足量的氨水:Al3++3OH-═Al(OH)3↓ |
| C、用小苏打治疗胃酸过多:HCO3-+H+═CO2↑+H2O |
| D、碳酸钡溶于醋酸:BaCO3+2H+═Ba2++H2O+CO2↑ |