题目内容
19.同温、同压下等质量的SO2气体和CO2气体,下列有关比较的叙述中不正确的是( )| A. | 物质的量比为11:16 | B. | 密度比为16:11 | ||
| C. | 体积比为16:11 | D. | 体积比为11:16 |
分析 A.根据n=$\frac{m}{M}$可知,等质量的二者的物质的量与摩尔质量成反比;
B.相同条件下密度与摩尔质量成正比;
C.相同条件下,气体摩尔体积相同,则二者的体积之比等于其物质的量之比;
D.相同条件下二者的气体摩尔体积相同,则等质量的二者的体积之比=物质的量之比.
解答 解:A.质量相等的SO2气体和CO2气体的物质的量与摩尔质量成反比,则等质量的二者的物质的量之比为:44g/mol:64g/mol=11:16,故A正确;
B.相同条件下,二氧化硫与二氧化碳的密度之比大于其摩尔质量之比=64g/mol:44g/mol=16:11,故B正确;
C.相同条件下具有相同的气体摩尔体积,则等质量的二者的体积之比等于其物质的量之比:11:16,故C错误;
D.根据C可知,二者的体积之比为:11:16,故D正确;
故选C.
点评 本题考查了阿伏伽德罗定律及其推论的综合应用,题目难度中等,明确阿伏伽德罗定律及推论的内容为解答关键,注意熟练掌握物质的量与摩尔质量、气体摩尔体积等物理量之间的关系,试题培养了学生的分子能力及化学计算能力.

练习册系列答案
相关题目
19.氢氧化钡(固体)、硫酸铜(固体)、硫酸(液体)这些物质可以归为一类,下列哪些物质还可以和它们归为一类( )
| A. | 豆浆 | B. | NaCl溶液 | C. | HCl | D. | 空气 |
20.下列说法错误的是( )
| A. | 某烃的分子式为 C10H14,它不能使溴水因反应而褪色,但可使酸性 KMnO4 溶液褪色,且分子结构中只有一个烷基,符合条件的芳香烃有 4 种(已知: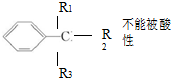 KMnO44氧化) KMnO44氧化) | |
| B. | 2,4-二甲基-3,3-二乙基戊烷的一氯代物有4种 | |
| C. | 甲烷与氯气的混合气体在光照条件下反应生成的有机化合物均无同分异构体 | |
| D. | 乙烷与丙烯的物质的量共 1mol,完全燃烧生成 3molH2O |
14.下列有关实验操作或判断正确的是( )
| A. | 为了便于操作,浓溶液稀释或固体溶解可直接在容量瓶中进行 | |
| B. | 需要95 mL 0.1 mol•L-1 NaCl溶液,可选用100 mL容量瓶来配制 | |
| C. | 用100 mL的量筒量取5.2 mL的盐酸 | |
| D. | 用托盘天平称取25.20 g NaCl |
11.下列反应中,属于取代反应的是( )
| A. | CH4+2 O2$\stackrel{点燃}{→}$CO2+H2O | |
| B. | CH2=CH2+HCl$\stackrel{一定条件}{→}$CH3CH2Cl | |
| C. | 2 CH3CH2OH+O2$→_{△}^{Cu}$2 CH3CHO+2 H2O | |
| D. | 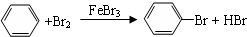 |
8.下列物质的分类中.正确的一组是( )
| 分类、选项 | 酸 | 碱 | 盐 | 碱性氧化物 |
| A | H2SO4 | Na2CO3 | NaHCO3 | CaO |
| B | HCl | NH3•H2O | NaCl | Na2O |
| C | CO2 | Cu(OH)2 | MgCl2 | Na2O |
| D | HNO3 | KOH | CaO | CO |
| A. | A | B. | B | C. | C | D. | D |
9.下列反应中,水既不是氧化剂又不是还原剂的氧化还原反应是( )
| A. | SO3+H2O═H2SO4 | B. | Cl2+H2O═HCl+HClO | ||
| C. | 2F2+2H2O═4HF+O2 | D. | 2Na+2H2O═2NaOH+H2↑ |
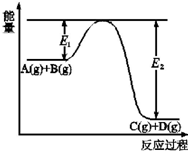 (1)1mol氢气在氯气中充分燃烧生成氯化氢气体时放出184.6kJ的热量,试写出对应的热化学方程式H2(g)+Cl2(g)=2HCl(g)△H=-184.6 kJ•mol-1.标准状况下11.2L氢气在氯气中充分燃烧放出的热量是92.3kJ.
(1)1mol氢气在氯气中充分燃烧生成氯化氢气体时放出184.6kJ的热量,试写出对应的热化学方程式H2(g)+Cl2(g)=2HCl(g)△H=-184.6 kJ•mol-1.标准状况下11.2L氢气在氯气中充分燃烧放出的热量是92.3kJ.