��Ŀ����
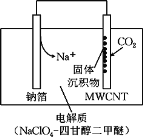
����Ŀ���ҹ�������Ա���Ƴ�һ���������ɺ�����Na��CO2��ء��ŵ�ʱ�õ����������CO2�����ʱ��������CO2������CO2ʱ���乤��ԭ����ͼ��ʾ�����յ�ȫ��CO2�У���![]() ת��ΪNa2CO3��������ڶ��̼���ܣ�MWCNT���缫���档����˵����ȷ���ǣ� ��
ת��ΪNa2CO3��������ڶ��̼���ܣ�MWCNT���缫���档����˵����ȷ���ǣ� ��
A.��������CO2ʱ��������Ӧ��4Na++ 3CO2+ 4e��= 2Na2CO3+ C
B.��������CO2ʱ���Ʋ�Ϊ����
C.��������CO2ʱ��Na+����̼���ܵ缫�ƶ�
D.��״���£�ÿ��������22.4 L CO2��ת�Ƶ�����Ϊ0.75 mol
���𰸡�A
��������
���ݵ缫���Ͽ�֪���ŵ�ʱ�Ʋ���������Ϊ������������CO2��һ��Ϊ����������ԭ��Ӧ��OԪ�ػ��ϼ�������ͼۣ�������CԪ�ر���ԭ����C���ʣ�ͬʱ���յ�CO2����![]() ת��ΪNa2CO3���壻���ʱ�Ʋ�Ϊ�����������ӱ���ԭΪNa�����̼����Ϊ������C���������̼��������CO2������CO2��
ת��ΪNa2CO3���壻���ʱ�Ʋ�Ϊ�����������ӱ���ԭΪNa�����̼����Ϊ������C���������̼��������CO2������CO2��
A�����ݷ�����֪��������CO2ʱ�����̼����Ϊ������CO2�õ��ӱ���ԭ��C���ʣ�ͬʱ�в��ֶ�����̼������������̼���ƣ����Ե缫��ӦʽΪ4Na++ 3CO2+ 4e��= 2Na2CO3+ C����A��ȷ��
B�����ݷ�����֪��������CO2ʱ���Ʋ�Ϊ��������B����
C����������CO2ʱΪ���أ������������������������������Ʋ��ƶ�����C����
D����״���£�22.4LCO2�����ʵ���Ϊ1mol�����ݷŵ�ʱ��������Ӧ��֪�����ʱ�����缫��ӦʽΪ2Na2CO3+C-4e-=4Na++3CO2������ÿ��������22.4 L CO2��ת�Ƶ�����Ϊ![]() mol����D����
mol����D����
��ѡA��

 ����ѵ��ϵ�д�
����ѵ��ϵ�д� ��ĩ�����ϵ�д�
��ĩ�����ϵ�д�