题目内容
【题目】不同元素的原子电负性不同,若用x值来表示,x值越大,其原子的电负性就越大,吸引电子的能力越强,在所形成的分子中成为带负电荷的一方,下面是某些短周期元素的电负性的值:
ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
第二周期 | Li | Be | B | C | N | O | F |
电负性值 | 0.98 | 1.57 | 2.04 | 2.55 | 3.44 | 3.98 | |
第三周期 | Na | Mg | Al | Si | P | S | Cl |
电负性值 | 0.93 | 1.61 | 1.90 | 2.19 | 2.58 | 3.16 |
(1)通过分析x值的变化规律,确定N、Mg的x值的范围:<x(Mg)< , <x(N)< .
(2)推测x值与原子半径的关系是 . 根据短周期元素x值变化特点,体现了元素性质的变化规律.
(3)某有机物结构简式如图,其中C﹣N中,你认为共用电子对偏向原子(填原子名称). 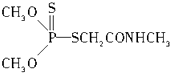
(4)经验规律告诉我们,当成键的两原子的x差值,即△x>1.7时,一般为离子键,当△x<1.7时,一般为共价键.试推断AlBr3中化学键的类型为
(5)预测元素周期表中x值最小的元素是(填元素符号,放射性元素除外).
【答案】
(1)0.93;1.57;2.55;3.44
(2)同周期(或同主族)元素,x值越大,原子半径越小;周期性
(3)氮
(4)共价键
(5)Cs
【解析】解:(1)由表中数值可看出,同周期中元素的x值随原子半径的减小而增大,同主族自上而下x值减小,x值的变化体现周期性的变化,故:0.93<x(Mg)<1.57,2.55<x(N)<3.44, 故答案为:0.93;1.57;2.55;3.44;(2)由表中数值可看出,同周期中元素的x值随原子半径的减小而增大,同主族自上而下原子半径增大,而x值减小,x值的变化体现周期性的变化,故答案为:同周期(或同主族)元素,x值越大,原子半径越小;周期性;(3)由于N的电负性等于碳的,故中C﹣N中共用电子对偏向氮原子,故答案为:氮;(4)由变化规律可知,Br的x值小于3.16,AlBr3中,Al元素与Br元素的△x<3.16﹣1.61=1.55<1.7,故AlBr3中化学键类型为共价键,故答案为:共价键;(5)同一周期周期从左到右,元素的x值最大,同一主族从上到下,x值逐渐减小,则x值最小的元素应位于周期表的左下角,排除放射性元素,应为Cs元素,故答案为:Cs.
(1)(2)题中给出的x值与吸引电子的能力有关,可根据元素周期性变化来推测Mg和N的x值,由表中数值可看出,同周期中元素的x值随原子半径的减小而增大,同主族自上而下x值减小,x值的变化体现周期性的变化;(3)电负性越大,对键合电子吸引越强;(4)由变化规律可知,Br的x值小于3.16,而△x>1.7时一般为离子键,当△x<1.7时一般为共价键;(5)同周期自左而右x值增大,同主族自上而下x减小.