题目内容
【题目】Ⅰ.在实验室利用下列装置,可制备某些气体并验证其化学性质。
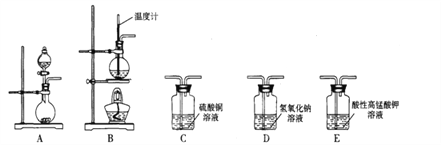
完成下列表格:
序号 | 气体 | 装置连接顺序(填字母) | 制备反应的化学方程式 |
(1) | 乙烯 | B→D→E | ________________ |
(2) | 乙炔 | ____________________ | _________________________ |
(3)D装置中氢氧化钠溶液的作用____________________________________。
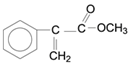
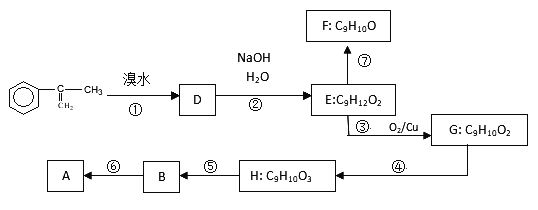
Ⅱ.工业上用乙烯和氯气为原料,经下列各步合成聚氯乙烯(PVC):

甲的结构简式是___________________________________________________;反应(3)的化学方程式是__________________________________________________。
【答案】 CH3CH2OH![]() CH2=CH2↑+ H2O A→C→E CaC2 + 2H2O → CH≡CH↑+ Ca(OH)2 除二氧化碳和二氧化硫 CH2Cl-CH2Cl
CH2=CH2↑+ H2O A→C→E CaC2 + 2H2O → CH≡CH↑+ Ca(OH)2 除二氧化碳和二氧化硫 CH2Cl-CH2Cl 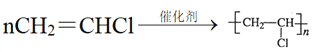
【解析】Ⅰ.(1)实验室利用乙醇能发生消去反应制乙烯,反应的方程式为CH3CH2OH![]() CH2=CH2↑+H2O;(2)实验室制取乙炔利用碳化钙与饱和食盐水反应,反应不需要加热,利用硫酸铜溶液除去乙炔中含有的杂质气体,利用酸性高锰酸钾溶液验证乙炔的性质,则装置连接顺序为A→C→E,发生反应的方程式为CaC2+2H2O→CH≡CH↑+Ca(OH)2;(3)在实验室中制取乙烯,需要加热到170℃,反应中会发生副反应生成二氧化硫和二氧化碳,必须用氢氧化钠溶液除去,即D装置中氢氧化钠溶液的作用是除二氧化碳和二氧化硫;
CH2=CH2↑+H2O;(2)实验室制取乙炔利用碳化钙与饱和食盐水反应,反应不需要加热,利用硫酸铜溶液除去乙炔中含有的杂质气体,利用酸性高锰酸钾溶液验证乙炔的性质,则装置连接顺序为A→C→E,发生反应的方程式为CaC2+2H2O→CH≡CH↑+Ca(OH)2;(3)在实验室中制取乙烯,需要加热到170℃,反应中会发生副反应生成二氧化硫和二氧化碳,必须用氢氧化钠溶液除去,即D装置中氢氧化钠溶液的作用是除二氧化碳和二氧化硫;
Ⅱ.CH2=CH2可与氯气发生加成反应生成CH2Cl-CH2Cl,CH2Cl-CH2Cl发生消去反应生成CH2=CHCl,CH2=CHCl发生加聚反应可生成PVC,反应(3)的方程式为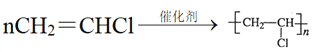 。
。

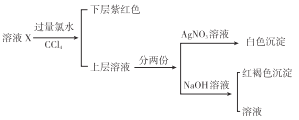
【题目】在探究新制氯水成分及性质的实验中,依据下列方法和现象,不能得出相应结论的是
方法 | 现象 | 结论 | |
A | 观察氯水颜色 | 氯水呈黄绿色 | 氯水中含Cl2 |
B | 向饱和NaHCO3溶液中加入足量氯水 | 有无色气体产生 | 氯水中含HClO |
C | 向红色纸条上滴加氯水 | 红色纸条褪色 | 氯水具有漂白性 |
D | 向FeCl2溶液中滴加氯水 | 溶液变成棕黄色 | 氯水具有氧化性 |
A. A B. B C. C D. D