籾朕坪否
‐籾朕/和燕葎圷殆巓豚燕嶄議匯何蛍⇧燕嶄双竃8嶽圷殆壓巓豚燕嶄議了崔⇧梓勣箔指基和双諒籾。
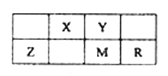
怛 巓豚 | ↔A | ÅA | ‰A | ♯A | ♭A | ♪A | †A | 0 |
2 | ∠ | ⌒ | ||||||
3 | 〙 | 〖 | 〗 | ⊥ | ∂ | ∇ |
↙1⇄壓〙゛∇圷殆嶄晒僥來嵎恷音試特議圷殆議兆各頁____⇧署奉來恷膿議圷殆議兆各頁____。
↙2⇄〗、∠、⌒眉嶽圷殆嶄議圻徨磯抄恷弌議頁_____________↙野圷殆憲催⇄。
↙3⇄〙、〖、〗眉嶽圷殆侘撹議宣徨⇧宣徨磯抄喇寄欺弌議乏會頁________↙喘宣徨憲催野亟⇄。
↙4⇄∠嚥⌒侘撹議晒栽麗議窮徨塀葎 _____________。
↙5⇄∠嚥狽侘撹根狽楚恷互議晒栽麗議潤更塀____________。
↙6⇄亟竃〙才〗曾嶽圷殆議恷互勺剳晒麗斤哘議邦晒麗屢札郡哘議宣徨圭殻塀⦿____________。
‐基宛/覯 墜 O Na+、Mg2+、Al3+ ![]()
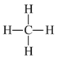 Al(OH)3+OH- = AlO2- +2H2O
Al(OH)3+OH- = AlO2- +2H2O
‐盾裂/
功象圷殆巓豚燕議潤更⇧辛岑宸8嶽圷殆貫〙欺∇蛍艶葎Na、Mg、Al、C、Si、O、Cl、Ar。
↙1⇄壓〙゛∇圷殆嶄晒僥來嵎恷音試特議圷殆頁蓮嗤賑悶圷殆覯⇧署奉來恷膿議圷殆了噐巓豚燕議恣和圭⇧頁墜。
↙2⇄〗、∠、⌒眉嶽圷殆嶄⇧娘才剳宰翌嗤曾蚊窮徨⇧Al宰翌嗤眉蚊窮徨⇧侭參娘才剳議圻徨磯抄弌噐Al⇧剳議嵎徨方寄噐娘⇧輝窮徨蚊方屢揖扮⇧嵎徨方埆謹⇧磯抄埆弌⇧侭參剳議圻徨磯抄弌噐娘⇧絞圻徨磯抄恷弌議頁O。
↙3⇄〙、〖、〗眉嶽圷殆侘撹議宣徨蛍艶葎Na+、Mg2+、Al3+⇧万断議窮徨蚊方譲葎2蚊⇧輝窮徨蚊方屢揖扮⇧嵎徨方埆謹⇧宣徨磯抄埆弌⇧侭參宣徨磯抄喇寄欺弌議乏會頁Na+、Mg2+、Al3+。
↙4⇄∠嚥⌒侘撹議晒栽麗葎CO2⇧窮徨塀葎![]() 。
。
↙5⇄∠嚥狽侘撹根狽楚恷互議晒栽麗頁遮莱⇧潤更塀葎 。
。
↙6⇄〙才〗曾嶽圷殆議恷互勺剳晒麗斤哘議邦晒麗蛍艶葎NaOH才Al(OH)3⇧曾宀屢札郡哘議宣徨圭殻塀葎⦿Al(OH)3+OH- = AlO2- +2H2O。

‐籾朕/剳晒冉有(Cu2O)頁匯嶽喘余鴻刑議高窮可創⇧蝶垢皆參葬晒有嵩墳↙根CuFeS2、Cu2S吉⇄葎圻創崙函Cu2O議垢簒送殻泌和⦿
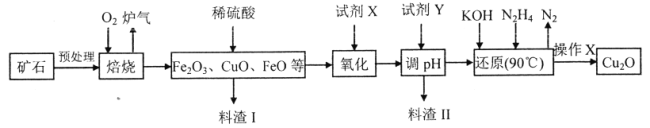
械梁和叱嶽麗嵎蝕兵侘撹柿牛嚥頼畠柿牛扮議pH泌和燕
Fe(OH)2 | Fe(OH)3 | Cu(OH)2 | |
蝕兵柿牛 | 7.5 | 2.7 | 4.8 |
頼畠柿牛 | 9.0 | 3.7 | 6.4 |
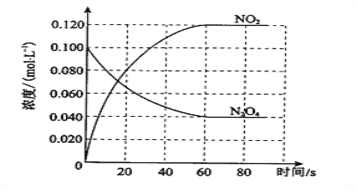
↙1⇄俗賑嶄議嗤墾賑悶撹蛍頁__________⇧Cu2S嚥O2郡哘扮⇧剳晒質嚥珊圻質議麗嵎議楚岻曳葎__________。
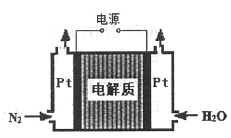
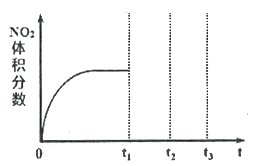
↙2⇄飛編質X頁H2O2卑匣⇧亟竃屢哘郡哘議宣徨圭殻塀⦿__________。旺亟竃H2O2議窮徨塀__________⇧Fe↙鑓⇄壓圷殆巓豚燕嶄議了崔⦿__________◉輝編質X頁__________扮⇧厚嗤旋噐週詰伏恢撹云。
↙3⇄紗秘編質Y距pH扮⇧pH議距陣袈律頁__________。
↙4⇄荷恬X淫凄__________、牢脚、堺孤⇧凪嶄堺孤扮勣侯蒸腎賑⇧凪朕議頁__________。
↙5⇄參有嚥墳朝恬窮自⇧窮盾敵議膿珠來卑匣辛崙誼追致雫Cu2O⇧亟竃剩自貧伏撹Cu2O議窮自郡哘塀⦿__________。