题目内容
【题目】下列说法可以证明反应N2(g)+3H2(g)![]() 2NH3(g)已达到平衡状态的是
2NH3(g)已达到平衡状态的是
A. 1个N≡N键断裂的同时,有3个H—H键形成
B. 1个N≡N键断裂的同时,有3个H—H键断裂
C. N2、H2、NH3的分子数之比为1∶3∶2
D. 1个N≡N键断裂的同时,有6个H—N键形成
【答案】A
【解析】试题分析:在一定条件下,当可逆反应的正反应速率和逆反应速率相等时(但不为0),反应体系中各种物质的浓度或含量不再发生变化的状态,称为化学平衡状态。则A、1个N≡N键断裂的同时,有3个H—H键形成,二者表示的反应速率分别是正逆反应速率,且满足化学计量数之比,因此说明反应达到平衡状态,A正确;B、1个N≡N键断裂的同时,有3个H—H键断裂均表示正反应速率,不能说明反应达到平衡状态,B错误;C、N2、H2、NH3的分子数之比为1∶3∶2不一定说明正逆反应速率相等,则不一定达到平衡状态,C错误;D、1个N≡N键断裂的同时,有6个H—N键形成均表示正反应速率,不能说明反应达到平衡状态,D错误,答案选A。

 一课一练一本通系列答案
一课一练一本通系列答案 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案【题目】实验室中有一未知浓度的稀盐酸,某学生测定盐酸的浓度在实验室中进行实验。请完成下列填空:
(1)配制100ml0.10molL1NaOH标准溶液,计算需称量_____g氢氧化钠固体。
(2)取20.00mL待测盐酸溶液放入锥形瓶中,并滴加23滴酚酞作指示剂,用自己配制的标准液NaOH溶液进行滴定。重复上述滴定操作23次,记录数据如下:
实验编号 | NaOH溶液的浓度 | 滴定完成时,NaOH溶液滴入的体积/mL | 待测盐酸的体积/mL |
1 | 0.10 | 22.62 | 20.00 |
2 | 0.10 | 22.72 | 20.00 |
3 | 0.10 | 22.80 | 20.00 |
①滴定达到终点的标志是____________________________________________.
②根据上述数据,可计算出该盐酸的浓度约为__________(保留两位有效数字).
③排去碱式滴定管中气泡的方法应采用如图所示操作中的________,然后轻轻挤压玻璃球使尖嘴部分充满碱液。

④在上述实验中,下列操作(其他操作正确)会造成测定结果偏高的有:___________
A. 滴定终点读数时俯视读数
B. 酸式滴定管使用前,水洗后未用待测盐酸溶液润洗
C. 锥形瓶水洗后未干燥
D. 称量NaOH固体中混有Na2CO3固体
E. 配制好的NaOH标准溶液保存不当,部分与空气中的CO2反应生成了Na2CO3
F. 碱式滴定管尖嘴部分有气泡,滴定后消失。
【题目】过氧乙酸(![]() )是一种高效消毒剂,常用于环境消毒杀菌,可以迅速杀死多种微生物。它可由冰醋酸和过氧化氢在浓硫酸催化作用下制得,实验装置和步骤如下:
)是一种高效消毒剂,常用于环境消毒杀菌,可以迅速杀死多种微生物。它可由冰醋酸和过氧化氢在浓硫酸催化作用下制得,实验装置和步骤如下:
①在三颈烧瓶中加入一定量冰醋酸与浓H2SO4的混合液体,再缓缓加入适量30%的双氧水。
②不断搅拌并控制B中混合液的温度为20~30℃至反应结束。
③接入冷凝管和抽气泵,在锥形瓶中收集得到产品。
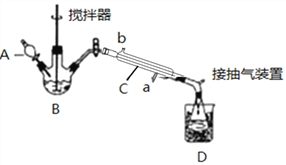
请回答下列问题:
(1)仪器C的名称是_______________;仪器C中冷水流入口是_____(填a或b);
(2)为更好地控制反应温度,应采用方法是_________________;
(3)生成过氧乙酸的化学方程式为________________________________________;
(4)不同反应物比例,实验测得生成过氧乙酸含量(%)随时间的变化数据(见下表),由表中数据可知,反应物最佳比例(CH3COOH/H2O2)是______,反应所需时间约________(选填1、3、5、7)小时;
反应物比例CH3COOH/H2O2 | 反应时间(小时) | ||||
0.5 | 1 | 3 | 5 | 7 | |
2:1 | 7.38 | 8.46 | 9.42 | 11.26 | 13.48 |
1:1 | 10.56 | 12.92 | 13.54 | 20.72 | 20.70 |
1:2 | 6.14 | 7.10 | 7.96 | 10.38 | 12.36 |
(5)请设计实验比较Fe3+、Cu2+对过氧乙酸的催化效率;可供选择的试剂和主要器材有:a.过氧乙酸溶液、b.1mol/L的FeCl3溶液、c.0.5mol/L的Fe2(SO4)3溶液、d.0.5mol/L的CuCl2溶液、e.1mol/L的CuSO4溶液、f.计时器、g.测量气体体积的针筒、i.带导气管的试管。
你选择的试剂及器材是a、_______、f、g、i(选填序号),实验方案是_________________________。
(6)碘量法分析:取2.00mL过氧乙酸试样稀释成