题目内容
【题目】对于反应14CuSO4 +5FeS2 +12H2O=7Cu2S +5FeSO4+12H2SO4,下列结论正确的是
A. FeS2既不是氧化剂,又不是还原剂
B. Cu2S 既是氧化产物,又是还原产物
C. 被氧化的硫和被还原的硫质量比是7∶3
D. 被CuSO4氧化的硫占全部被氧化的硫的2/3
【答案】D
【解析】A.该反应中Cu元素化合价由+2价变为+1价、S元素化合价由-1价变为+6价、-2价,Cu元素被还原、S元素既被氧化,又被还原,则FeS2既是氧化剂,又是还原剂,A错误;B.根据元素化合价知,Cu2S只是还原产物,B错误;C.被氧化的S和被还原的S质量比为3:7,C错误;D.1mol硫酸铜失去1mol电子,被硫酸铜氧化的S是1/7mol,而1mol硫酸铜参加反应被氧化的硫是![]() ,所以被CuSO4氧化的硫占全部被氧化的硫的
,所以被CuSO4氧化的硫占全部被氧化的硫的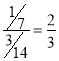 ,D正确,答案选D。
,D正确,答案选D。

练习册系列答案
 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案
相关题目