��Ŀ����
��8�֣�ijУ��ѧ�о���ѧϰС�������ʵ����֤Fe��Cu�Ľ�����ԣ�����������������ַ��������������������й�ʵ����Ŀ��
������:�����������С��ȵ���Ƭ��ͭƬ���ֱ�ͬʱ����ϡ���ᣨ��ϡ���ᣩ�У��۲�������ݵĿ������ݴ�ȷ�����ǵĻ�ԡ���ԭ�������ӷ���ʽΪ ��
��������������Fe��Cu���缫��Ƴ�ԭ��أ���ȷ�����ǵĻ�ԡ���������ķ����ڻ���ԭ���װ��ͼ�����ԭ��صĵ缫���Ϻ͵������Һ����д���缫��Ӧʽ��

������Ӧʽ�� ��������Ӧʽ�� ��
���õ������0.1mol�ĵ���ת�ƣ��������� ��Fe
�����������ѧ��֪ʶ���������������һ����֤Fe��Cu��Եļ�ʵ�鷽�����뷽��������ͬ���� __________________�������ӷ���ʽ��ʾ�䷴Ӧԭ���� ______________
����8�֣�
������Fe+2H+=Fe2++H2����1�֣�
��������װ��ͼ��ȫ��ȷ2�֣������ľ����֣�

2H++2e- =H2����1�֣� Fe-2e-=Fe2+��1�֣� 2.8 g
��������Ƭ����CuSO4��Һ�У�һ��ʱ��۲���Ƭ�����Ƿ����ɺ�ɫ���ʣ�1�֣�Fe+Cu2+ = Cu+Fe2+��1�֣�
�������������Ļ���ж�����֤������������ˮ�����û����������������������ˮ����ļ���ǿ����ԭ���ԭ�������ԭ����Ӧ�á�����֮����û��ȵȡ�

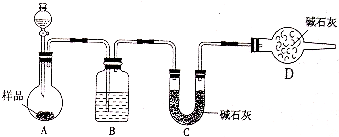

 ijУ��ѧ�о���ѧϰС���������ʵ�鷽�����ⶨ���ü��õ�С�մ���Ʒ�д��������������
ijУ��ѧ�о���ѧϰС���������ʵ�鷽�����ⶨ���ü��õ�С�մ���Ʒ�д��������������